NAD+ 前體煙酰胺單核苷酸 (NMN) 和煙酰胺核苷 (NR):
飲食對健康的潛在貢獻(2023/01)
摘要
審查目的
NAD+ 是一種重要的分子,除了在能量、基因毒性和傳染性應激的調節通路中用作重要細胞信號轉導的底物外,還作為氧化還原輔助因子參與多種代謝反應。 在壓力條件下,NAD+ 生物合成和水平降低,消耗酶的活性升高。 膳食前體可以促進 NAD+ 生物合成並增加細胞內水平,是逆轉生理衰退和預防疾病的潛在策略。 在這篇綜述中,我們將展示 NAD+ 前體 NR(煙酰胺核苷)和 NMN(煙酰胺單核苷酸)的生物化學和代謝、它們有益生理作用的最新發現、它們與腸道微生物群的相互作用,以及營養和營養研究的未來前景 食品科學領域。
最近的發現
NMN 和 NR 被證明可以預防糖尿病、阿爾茨海默病、內皮功能障礙和炎症。 它們還可以逆轉腸道菌群失調,並促進腸道和腸外水平的有益作用。 NR和NMN已在蔬菜、肉類和牛奶中發現,發酵飲料中的微生物也能產生。
概括
NMN 和 NR 可以通過飲食以游離形式或從 NAD+ 消化中衍生的代謝物形式獲得。 NR 和 NMN 尋找潛在食物來源的前景及其在增加 NAD+ 水平方面的飲食貢獻仍然是一個未開發的研究領域。 此外,除了用於提取和生物技術開發的新原料研究之外,它還可以開發新的功能性食品和加工策略以保持和增強其生理益處。
簡介
NAD+ 是一種重要的分子,除了在能量、基因毒性和傳染性應激的調節通路中用作重要細胞信號轉導的底物外,還作為氧化還原輔助因子參與多種代謝反應。 在壓力條件下,NAD+ 生物合成和水平降低,消耗酶的活性升高。 膳食前體可以促進 NAD+ 生物合成並增加細胞內水平,是逆轉生理衰退和預防疾病的潛在策略。 在這篇綜述中,我們將展示 NAD+ 前體 NR(煙酰胺核苷)和 NMN(煙酰胺單核苷酸)的生物化學和代謝、它們有益生理作用的最新發現、它們與腸道微生物群的相互作用,以及營養和營養研究的未來前景 食品科學領域。
最近的發現
NMN 和 NR 被證明可以預防糖尿病、阿爾茨海默病、內皮功能障礙和炎症。 它們還可以逆轉腸道菌群失調,並促進腸道和腸外水平的有益作用。 NR和NMN已在蔬菜、肉類和牛奶中發現,發酵飲料中的微生物也能產生。
概括
NMN 和 NR 可以通過飲食以游離形式或從 NAD+ 消化中衍生的代謝物形式獲得。 NR 和 NMN 尋找潛在食物來源的前景及其在增加 NAD+ 水平方面的飲食貢獻仍然是一個未開發的研究領域。 此外,除了用於提取和生物技術開發的新原料研究之外,它還可以開發新的功能性食品和加工策略以保持和增強其生理益處。
簡介
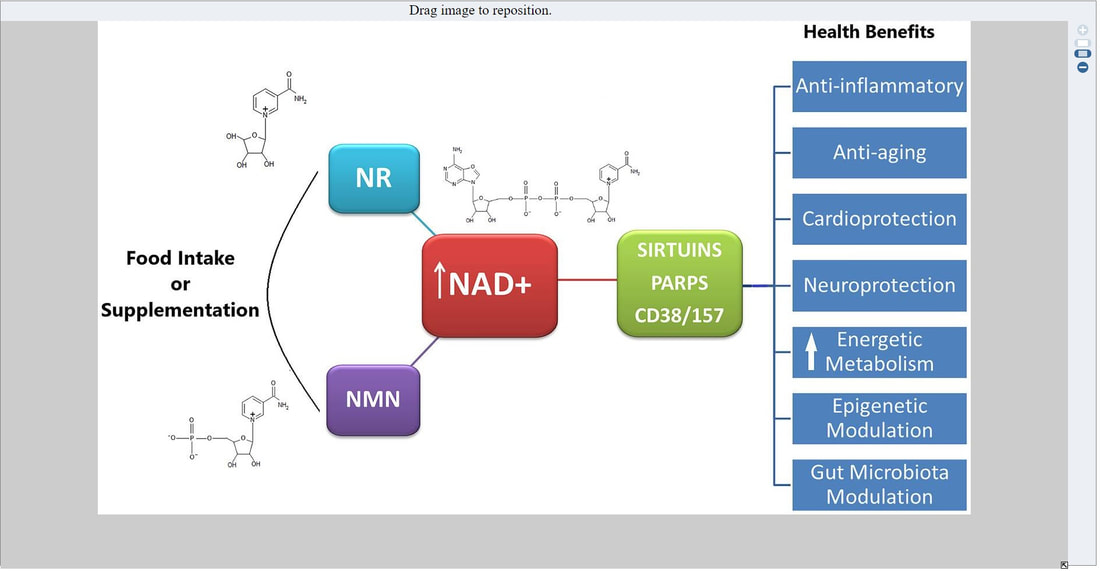
NAD+ 是煙酰胺腺嘌呤二核苷酸的氧化形式,是生物體維持細胞健康所必需的分子。 它已被證明可以促進多種健康益處,包括增強能量代謝、心臟和神經保護、DNA 修復以及抗炎和抗衰老作用。
除了作為接受電子進行分解代謝反應的輔酶在能量代謝中發揮關鍵作用外,NAD+ 還作為共底物參與細胞內鈣動員和翻譯後蛋白質修飾的信號通路 。 這些由 NAD+ 介導的重要細胞過程的調節賦予線粒體功能保護、氧化還原穩態控制、抗炎作用、減輕與年齡相關的功能障礙、細胞分化、基因組穩定性和表觀遺傳調節等。
NAD+ 在細胞中不斷合成、分解代謝和循環,以維持穩定的水平。 衰老以及高脂肪和蛋白質攝入導致的營養過剩 等干擾會影響 NAD+ 的合成,並與這種重要分子的水平降低有關。 低 NAD+ 水平是生理衰退和年齡相關疾病(如神經退行性、代謝和眼部疾病)發作的標誌之一 。 同樣,NAD+ 耗竭與並發症和冠狀病毒疾病 (Covid-19) 的惡化有關。 總之,NAD+ 下降可能是由於 NAD 合成酶減少、NAD 消耗酶增加或兩者兼而有之。
通過生物合成前體提高 NAD+ 水平有可能預防或減輕多種疾病,例如代謝和與年齡相關的疾病。 基於它們提高 NAD+ 水平的能力,煙酰胺核苷 (NR) 和煙酰胺單核苷酸 (NMN) 已被證明可以減輕生理衰退、糖尿病和糖尿病性神經病變,防止肝脂肪變性,減少阿爾茨海默病的各種病理特徵 ,保護神經元細胞免受氧化應激,並保持認知能力 。 此外,它們在急性腎功能衰竭、抗炎、心臟和血管保護作用、端粒延長、延長壽命和促進健康方面表現出有益的藥理活性 在各種生物體中,從酵母到哺乳動物。
NMN 和 NR 補充劑已成為臨床試驗的主題,以評估其在人體中的安全性和適用性。 然而,這些 NAD+ 前體也存在於食品中,可能具有潛在的飲食治療作用,類似於酚類和其他生物活性食品化合物。 來自蔬菜、肉類和牛奶中 NMN 和 NR 存在的證據強化了它們的自然存在 ,儘管關於食品中 NMN 和 NR 含量的數據仍然有限。 到目前為止,毛豆、鱷梨和西蘭花等植物來源的含量略高; 研究對於確定最佳食物來源並確定正常飲食是否提供足夠數量的這些前體以增加 NAD+ 水平至關重要。 這些新型 NAD+ 前體在食物來源中的分佈呈現了一個令人興奮的新研究領域,特別是關於它們通過飲食對健康促進的潛在貢獻。
此外,值得注意的是腸道微生物群與 NAD+代謝物之間的聯繫對宿主整體健康的潛在影響。 雖然棲息在腸道中的微生物在 NAD+及其代謝物的代謝中發揮作用,但 NMN 和 NR 也會影響腸道微生物群的組成,逆轉腸道菌群失調並促進腸道和腸外水平的有益作用。
因此,本綜述將涵蓋 NAD+⟩前體 NMN 和 NR 的生物化學和代謝,以及它們最新的有益生理效應、與腸道菌群的相互作用以及在營養和食品科學領域的未來研究前景。
NAD+、NMN 和 NR 代謝
除了作為接受電子進行分解代謝反應的輔酶在能量代謝中發揮關鍵作用外,NAD+ 還作為共底物參與細胞內鈣動員和翻譯後蛋白質修飾的信號通路 。 這些由 NAD+ 介導的重要細胞過程的調節賦予線粒體功能保護、氧化還原穩態控制、抗炎作用、減輕與年齡相關的功能障礙、細胞分化、基因組穩定性和表觀遺傳調節等。
NAD+ 在細胞中不斷合成、分解代謝和循環,以維持穩定的水平。 衰老以及高脂肪和蛋白質攝入導致的營養過剩 等干擾會影響 NAD+ 的合成,並與這種重要分子的水平降低有關。 低 NAD+ 水平是生理衰退和年齡相關疾病(如神經退行性、代謝和眼部疾病)發作的標誌之一 。 同樣,NAD+ 耗竭與並發症和冠狀病毒疾病 (Covid-19) 的惡化有關。 總之,NAD+ 下降可能是由於 NAD 合成酶減少、NAD 消耗酶增加或兩者兼而有之。
通過生物合成前體提高 NAD+ 水平有可能預防或減輕多種疾病,例如代謝和與年齡相關的疾病。 基於它們提高 NAD+ 水平的能力,煙酰胺核苷 (NR) 和煙酰胺單核苷酸 (NMN) 已被證明可以減輕生理衰退、糖尿病和糖尿病性神經病變,防止肝脂肪變性,減少阿爾茨海默病的各種病理特徵 ,保護神經元細胞免受氧化應激,並保持認知能力 。 此外,它們在急性腎功能衰竭、抗炎、心臟和血管保護作用、端粒延長、延長壽命和促進健康方面表現出有益的藥理活性 在各種生物體中,從酵母到哺乳動物。
NMN 和 NR 補充劑已成為臨床試驗的主題,以評估其在人體中的安全性和適用性。 然而,這些 NAD+ 前體也存在於食品中,可能具有潛在的飲食治療作用,類似於酚類和其他生物活性食品化合物。 來自蔬菜、肉類和牛奶中 NMN 和 NR 存在的證據強化了它們的自然存在 ,儘管關於食品中 NMN 和 NR 含量的數據仍然有限。 到目前為止,毛豆、鱷梨和西蘭花等植物來源的含量略高; 研究對於確定最佳食物來源並確定正常飲食是否提供足夠數量的這些前體以增加 NAD+ 水平至關重要。 這些新型 NAD+ 前體在食物來源中的分佈呈現了一個令人興奮的新研究領域,特別是關於它們通過飲食對健康促進的潛在貢獻。
此外,值得注意的是腸道微生物群與 NAD+代謝物之間的聯繫對宿主整體健康的潛在影響。 雖然棲息在腸道中的微生物在 NAD+及其代謝物的代謝中發揮作用,但 NMN 和 NR 也會影響腸道微生物群的組成,逆轉腸道菌群失調並促進腸道和腸外水平的有益作用。
因此,本綜述將涵蓋 NAD+⟩前體 NMN 和 NR 的生物化學和代謝,以及它們最新的有益生理效應、與腸道菌群的相互作用以及在營養和食品科學領域的未來研究前景。
NAD+、NMN 和 NR 代謝
在真核生物中,NAD+ 執行兩個重要功能:能量轉導和細胞信號傳導。 NAD+ 最初是作為 ATP(三磷酸腺苷)合成的重要氧化還原輔因子而建立的。 隨後,NAD+ 降解過程被揭示,將其用作 CD38/CD157/SARM1、ADP-核糖基轉移酶 (ART)、多聚 ADP 聚合酶 (PARP) 和去乙酰化酶 的底物(圖 1) . 這些 NAD 依賴性酶介導機體穩態的基本細胞過程,例如 DNA 修復、細胞凋亡、細胞存活 、壽命調節、代謝調節、炎症和感染。
NAD+ 是由焦磷酸基團連接的兩個核苷組成的吡啶核苷酸。 每個核苷都包含一個核糖環,其中一個核苷含有連接到第一個碳原子的腺嘌呤(二磷酸腺苷核糖),另一個核苷在相同位置含有煙酰胺 (NMN)(圖 1)。
NAD+ 合成可由色氨酸和維生素 B3(菸酸和煙酰胺)產生。 後來,中間體 NR 和 NMN 也被確定可促進 NAD+ 合成 。 NR 是一種吡啶核苷,由胺(煙酰胺)和核糖的 β-N-糖苷鍵組成。 NMN 是一種吡啶核苷酸,它包含一個與磷酸基團結合的 NR 分子。 NMN 和 NR 參與 NAD+ 的降解和再合成(圖 1),NAD+ 的這種代謝循環因物種和界而異 。
在哺乳動物中,NAD 可以通過不同的方式產生:通過氨基酸色氨酸的從頭生成,通過補救途徑中的煙酰胺 (NAM) 作為 NAD 循環系統從這些消耗反應中釋放出來,或者通過菸酸/菸酸 (NA) 在 Preiss-Handler 通路中(圖 2A)。 前體酰胺化煙酰胺 (NAM)、NMN 和 NR 是補救途徑中的主要底物。 此外,最近,NR 和 NMN 的還原形式,即二氫煙酰胺核苷 (NRH) 和二氫煙酰胺單核苷酸 (NMNH),也被證明可以促進合成(圖 2A)。
NAD+ 合成可由色氨酸和維生素 B3(菸酸和煙酰胺)產生。 後來,中間體 NR 和 NMN 也被確定可促進 NAD+ 合成 。 NR 是一種吡啶核苷,由胺(煙酰胺)和核糖的 β-N-糖苷鍵組成。 NMN 是一種吡啶核苷酸,它包含一個與磷酸基團結合的 NR 分子。 NMN 和 NR 參與 NAD+ 的降解和再合成(圖 1),NAD+ 的這種代謝循環因物種和界而異 。
在哺乳動物中,NAD 可以通過不同的方式產生:通過氨基酸色氨酸的從頭生成,通過補救途徑中的煙酰胺 (NAM) 作為 NAD 循環系統從這些消耗反應中釋放出來,或者通過菸酸/菸酸 (NA) 在 Preiss-Handler 通路中(圖 2A)。 前體酰胺化煙酰胺 (NAM)、NMN 和 NR 是補救途徑中的主要底物。 此外,最近,NR 和 NMN 的還原形式,即二氫煙酰胺核苷 (NRH) 和二氫煙酰胺單核苷酸 (NMNH),也被證明可以促進合成(圖 2A)。

圖二
人類 (A) 和植物 (B) 中的 NAD 生物合成途徑。 NMN 可以通過 CD73 介導的去磷酸化為 NR,或通過基因 SLC12A8 編碼的轉運蛋白被攝取。 虛線箭頭表示假定的途徑。 前體/代謝物:KYN:N-甲酰犬尿氨酸; NMN(煙酰胺單核苷酸); NMNH(二氫煙酰胺單核苷酸); NR(煙酰胺核苷); NRH(二氫煙酰胺核苷); NAR(菸酸核苷); NAM(煙酰胺); NA(菸酸); NAMN(菸酸單核苷酸); NAAD(菸酸腺嘌呤二核苷酸)、QA(喹啉酸); TRYP(色氨酸)。 酶:AK,腺苷激酶; CD73/CD38/CD157,外生酶; IDO,吲哚胺 2,3-雙加氧酶; NADPPase(NAD焦磷酸酶); NADS(NAD合酶); NAMPT,煙酰胺磷酸核糖轉移酶; NAPT(菸酸磷酸核糖基轉移酶); NARK(菸酸核糖激酶); NIC(煙酰胺酶); NMNAT(煙酰胺/菸酸單核苷酸腺苷酸轉移酶); NRase(煙酰胺核苷核苷酶); NRD(煙酰胺核苷脫氨酶); NRK1/2:煙酰胺核苷激酶; NUDase(5'-核苷酸酶); PARPs,poli-ADPR 聚合酶; PNP,嘌呤核苷磷酸化酶; QPRTase:QA-磷酸核糖基轉移酶; SIRT、sirtuins、TDO、色氨酸 2,3-雙加氧酶。
Image created with https://www.biorender.com/
此外,值得一提的是微生物群在 NAD+ 合成中的作用。 與哺乳動物不同,腸道中存在的細菌擁有通過脫酰胺過程將 NMN 轉化為菸酸單核苷酸 (NAMN) 的酶。 之後,NAMN 通過 Preiss-Handler 途徑進行 NAD+ 合成。 在大鼠中口服給藥的同位素標記的 NMN 在吸收前被腸道微生物群部分脫酰胺為 NAMN。 儘管明顯低於酰胺化代謝物 NMN 和 NAD+,但肝臟中的菸酸腺嘌呤二核苷酸 (NAAD) 水平增加了,正如在補充 NR 時觀察到的那樣,這導致 NAAD 增加 。NAM 和 NR 對 NAD+ 的增強主要是通過微生物群依賴性脫酰胺途徑。
此外,NR 可以通過兩種不同的方式增加 NAD+ 水平。 通過補救途徑直接吸收,或被糖水解酶骨髓基質細胞抗原 1 (BST1) 水解為煙酰胺 (NAM),然後通過 Preiss–Handler 途徑被腸道微生物群進一步代謝為菸酸。 此外,據報導,BST1 對 NR 和菸酸核苷 (NAR) 均具有鹼基交換活性,可分別生成 NAR 和 NR,從而連接酰胺化和脫酰胺化途徑 。
因此,有幾種途徑允許使用替代前體來維持細胞內 NAD 水平。 這種冗餘是至關重要的還是具有特定於組織的重要性仍未得到探索。
NMN 和 NR 的來源
此外,NR 可以通過兩種不同的方式增加 NAD+ 水平。 通過補救途徑直接吸收,或被糖水解酶骨髓基質細胞抗原 1 (BST1) 水解為煙酰胺 (NAM),然後通過 Preiss–Handler 途徑被腸道微生物群進一步代謝為菸酸。 此外,據報導,BST1 對 NR 和菸酸核苷 (NAR) 均具有鹼基交換活性,可分別生成 NAR 和 NR,從而連接酰胺化和脫酰胺化途徑 。
因此,有幾種途徑允許使用替代前體來維持細胞內 NAD 水平。 這種冗餘是至關重要的還是具有特定於組織的重要性仍未得到探索。
NMN 和 NR 的來源
生物合成 NAD+ 前體可以通過飲食或補充獲得。 前體色氨酸、NAM、NA、NMN 和 NR 可以通過飲食以游離形式獲得,也可以作為 NAD+ 消化的代謝產物衍生物獲得。
NR 與 NAM 和 NA 一起被命名為第三種 NAD+ 維生素前體。 測量食品中 NA 含量的官方方法之一是微生物檢測。 在評估中,食品基質在高溫下進行酸或鹼處理(AOAC 方法 944.13)。 眾所周知,在這些條件下,NAM、NAD 和 NADP 會轉化為 NA,鹼處理會釋放 NA,最終與多醣、肽或糖肽結合。 烏馬里諾等人。 (2017) 調查了 NMN 和 NR 在暴露於熱酸或鹼提取程序時是否也會產生 NA。 事實上,NR 和 NMN 分子被水解成 NA,並且可以解釋所分析的牛奶樣品中的總菸酸含量。 因此,這表明通過微生物測定量化的菸酸包括最終存在於食物基質中的 NR 和 NMN。
雖然 NMN 和 NR 可以在動物源性食品和蘑菇中找到,但本節將重點關注它們在植物中的含量,作為一種潛在的良好膳食來源,因為正在進行的實驗(結果未發表)支持這一觀點。
NAD+對於植物適應紫外線照射、鹽度、熱休克和乾旱脅迫等環境脅迫至關重要。 此外,NAD+參與植物生物學的幾個關鍵因素,包括生長和發育、代謝(能量、活性氧和氮物質、收穫)、信號傳導、基因表達、免疫和生物合成 。 基因轉錄研究揭示了果實發育和生長過程中的不同表達模式。 在與 NAD 代謝相關的特定基因中,從頭途徑生物合成基因在幼番茄中被轉錄誘導。 果實生長的後期階段顯示參與補救途徑的基因積累,這與 NAD 水平增加相吻合,最有可能在成熟過程中維持高代謝活性。
在植物中,NAD 通過氨基酸天冬氨酸的從頭合成途徑和補救途徑合成; 然而,菸酸 (NA) 是吡啶核苷酸循環的關鍵代謝物(圖 2B)。 以前,由七種代謝物組成的 NAD+ 生物合成途徑最為人所知; 然而,在馬鈴薯塊莖中發現了一個包含煙酰胺核苷脫氨酶的循環。 新循環繞過了煙酰胺和菸酸途徑(圖 2B),表明它可能發生在某些植物物種中 。
NMN 是通過 NAD+ 二磷酸酶 的作用打破 NAD+分子的二磷酸鏈而產生的,例如 nudix 水解酶,也稱為 NAD 焦磷酸酶。 儘管 6 步或 8 步脫酰胺的補救途徑最為普遍,但 NMN 也可以通過煙酰胺單核苷酸腺苷酸轉移酶 (NMNAT) 催化的一步在植物中轉化為 NAD。 菊芋 (Helianthus tuberosus L.) 證實了線粒體部分中特異性的 NMNAT 活性,並在 NAD 代謝中發揮重要作用 。 在扁豆和仙人掌(仙人掌)中,核苷酸焦磷酸酶被鑑定出來,並在 NAD(P) 的還原和氧化形式的焦磷酸鍵上表現出水解活性,產生 NMN 和 AMP. 在茶葉、馬鈴薯、裸子植物和豆科植物等植物中,5'核苷酸酶活性將 NMN 轉化為 NR 。 這些發現將 NMN 和 NR 描述為植物 NAD+ 池的代謝物,而植物性食物則是這些化合物的來源。
因此,哺乳動物通過膳食 NAD+的消化分解暴露於這些前體。 生物利用度研究表明,攝入的 NAD+主要在小腸中被存在於刷狀緣細胞或腸道分泌物中的焦磷酸酶水解。 腸道中轉運蛋白的表達強化了 NMN 可以通過口服遞送實現生物利用。
迄今為止,只有少數研究測量了食品中的 NMN 和 NR,因此尚未明確確定最佳來源。 米爾斯等人。 (2016) 發表了 NMN 在毛豆、鱷梨、西蘭花、黃瓜、捲心菜和番茄等食物中的第一個證據。 在調查的來源中,毛豆中含量最高,範圍為 0.47-1.88(毫克/100 克),鱷梨含量為 0.36-1.60(毫克/100 克),海鮮和生肉中含量較少(0.06-0.42 毫克) /100 克) 。 此外,還在不同種類的牛奶和啤酒中測定了 NR 和 NMN 。 自從首次在牛奶中發現 NR 以來,迄今為止僅在牛奶中對其進行了測量,其中牛奶的含量最高 (0.5–3.6 μM) 和人乳作為最豐富的 NMN 來源 (2.1–9.8 μM) 。 由於摩爾濃度通常以每升溶液中溶質的摩爾數為單位表示,因此假設濃度是針對 1 升牛奶的體積,因為參考文章中未說明此信息。
最近,酵母介導的精釀啤酒中的 NR 和 NMN 生產得到證實,啤酒花表明在發酵過程中提高 NR 水平的作用; 因此,通過發酵食品和飲料為豐富的 NAD+ 前體來源開闢了新的視角。 這將帶來新的可能性以及微生物物種(例如,嗜果性乳酸菌)的潛在生物技術用途,以生產用於功能性益生菌產品和補充劑的 NMN 和 NR 。
最後,NMN 和 NR 以膠囊或粉末形式以高價銷售,劑量範圍為 100 至 1000 毫克,這是研究中每天使用的劑量。 然而,重要的是要注意,人類尚未完全了解 NMN 和 NR 補充劑的最佳劑量,需要進一步研究以確定最有效和安全的劑量。 通過飲食獲取 NAD+ 前體可能是一種更容易獲得和更自然的替代方法,儘管與補充劑相比,它們在食物來源中的含量較低。 需要進一步的研究來澄清這些問題。
安全性和藥代動力學
NR 與 NAM 和 NA 一起被命名為第三種 NAD+ 維生素前體。 測量食品中 NA 含量的官方方法之一是微生物檢測。 在評估中,食品基質在高溫下進行酸或鹼處理(AOAC 方法 944.13)。 眾所周知,在這些條件下,NAM、NAD 和 NADP 會轉化為 NA,鹼處理會釋放 NA,最終與多醣、肽或糖肽結合。 烏馬里諾等人。 (2017) 調查了 NMN 和 NR 在暴露於熱酸或鹼提取程序時是否也會產生 NA。 事實上,NR 和 NMN 分子被水解成 NA,並且可以解釋所分析的牛奶樣品中的總菸酸含量。 因此,這表明通過微生物測定量化的菸酸包括最終存在於食物基質中的 NR 和 NMN。
雖然 NMN 和 NR 可以在動物源性食品和蘑菇中找到,但本節將重點關注它們在植物中的含量,作為一種潛在的良好膳食來源,因為正在進行的實驗(結果未發表)支持這一觀點。
NAD+對於植物適應紫外線照射、鹽度、熱休克和乾旱脅迫等環境脅迫至關重要。 此外,NAD+參與植物生物學的幾個關鍵因素,包括生長和發育、代謝(能量、活性氧和氮物質、收穫)、信號傳導、基因表達、免疫和生物合成 。 基因轉錄研究揭示了果實發育和生長過程中的不同表達模式。 在與 NAD 代謝相關的特定基因中,從頭途徑生物合成基因在幼番茄中被轉錄誘導。 果實生長的後期階段顯示參與補救途徑的基因積累,這與 NAD 水平增加相吻合,最有可能在成熟過程中維持高代謝活性。
在植物中,NAD 通過氨基酸天冬氨酸的從頭合成途徑和補救途徑合成; 然而,菸酸 (NA) 是吡啶核苷酸循環的關鍵代謝物(圖 2B)。 以前,由七種代謝物組成的 NAD+ 生物合成途徑最為人所知; 然而,在馬鈴薯塊莖中發現了一個包含煙酰胺核苷脫氨酶的循環。 新循環繞過了煙酰胺和菸酸途徑(圖 2B),表明它可能發生在某些植物物種中 。
NMN 是通過 NAD+ 二磷酸酶 的作用打破 NAD+分子的二磷酸鏈而產生的,例如 nudix 水解酶,也稱為 NAD 焦磷酸酶。 儘管 6 步或 8 步脫酰胺的補救途徑最為普遍,但 NMN 也可以通過煙酰胺單核苷酸腺苷酸轉移酶 (NMNAT) 催化的一步在植物中轉化為 NAD。 菊芋 (Helianthus tuberosus L.) 證實了線粒體部分中特異性的 NMNAT 活性,並在 NAD 代謝中發揮重要作用 。 在扁豆和仙人掌(仙人掌)中,核苷酸焦磷酸酶被鑑定出來,並在 NAD(P) 的還原和氧化形式的焦磷酸鍵上表現出水解活性,產生 NMN 和 AMP. 在茶葉、馬鈴薯、裸子植物和豆科植物等植物中,5'核苷酸酶活性將 NMN 轉化為 NR 。 這些發現將 NMN 和 NR 描述為植物 NAD+ 池的代謝物,而植物性食物則是這些化合物的來源。
因此,哺乳動物通過膳食 NAD+的消化分解暴露於這些前體。 生物利用度研究表明,攝入的 NAD+主要在小腸中被存在於刷狀緣細胞或腸道分泌物中的焦磷酸酶水解。 腸道中轉運蛋白的表達強化了 NMN 可以通過口服遞送實現生物利用。
迄今為止,只有少數研究測量了食品中的 NMN 和 NR,因此尚未明確確定最佳來源。 米爾斯等人。 (2016) 發表了 NMN 在毛豆、鱷梨、西蘭花、黃瓜、捲心菜和番茄等食物中的第一個證據。 在調查的來源中,毛豆中含量最高,範圍為 0.47-1.88(毫克/100 克),鱷梨含量為 0.36-1.60(毫克/100 克),海鮮和生肉中含量較少(0.06-0.42 毫克) /100 克) 。 此外,還在不同種類的牛奶和啤酒中測定了 NR 和 NMN 。 自從首次在牛奶中發現 NR 以來,迄今為止僅在牛奶中對其進行了測量,其中牛奶的含量最高 (0.5–3.6 μM) 和人乳作為最豐富的 NMN 來源 (2.1–9.8 μM) 。 由於摩爾濃度通常以每升溶液中溶質的摩爾數為單位表示,因此假設濃度是針對 1 升牛奶的體積,因為參考文章中未說明此信息。
最近,酵母介導的精釀啤酒中的 NR 和 NMN 生產得到證實,啤酒花表明在發酵過程中提高 NR 水平的作用; 因此,通過發酵食品和飲料為豐富的 NAD+ 前體來源開闢了新的視角。 這將帶來新的可能性以及微生物物種(例如,嗜果性乳酸菌)的潛在生物技術用途,以生產用於功能性益生菌產品和補充劑的 NMN 和 NR 。
最後,NMN 和 NR 以膠囊或粉末形式以高價銷售,劑量範圍為 100 至 1000 毫克,這是研究中每天使用的劑量。 然而,重要的是要注意,人類尚未完全了解 NMN 和 NR 補充劑的最佳劑量,需要進一步研究以確定最有效和安全的劑量。 通過飲食獲取 NAD+ 前體可能是一種更容易獲得和更自然的替代方法,儘管與補充劑相比,它們在食物來源中的含量較低。 需要進一步的研究來澄清這些問題。
安全性和藥代動力學
正在進行多項研究以評估補充 NMN 和 NR 的生理效應,包括人體安全性和藥代動力學(NCT04228640、NCT04910061)、衰老(NCT04823260、NCT04685096)、高血壓(NCT04903210)、心力衰竭(NCT03565328、NCT04528004)、 關於 COVID-19(NCT04407390、NCT05175768、NCT04818216)、關於線粒體功能(NCT03789175、NCT03951285)、代謝和心血管功能(NCT04571008)、骨骼肌和骨代謝功能(NCT03818802、NCT04691986)、關於肌肉生理學和身體能力(NCT04691986, NCT04664361),以及其他(在數據庫 ClinicalTrials.Gov 中列出)。 儘管補充 NR 和 NMN 的臨床前和臨床試驗結果很有希望,但仍需要確定長期補充和高劑量是否會出現副作用。
例如,NAMPT 抑制導致的 NAD 合成抑制會降低細胞生長並增加對氧化應激的易感性,這已成為癌症治療的一個治療概念。 雖然 NAD+ 前體 NMN 和 NR 可逆轉 NAMPT 抑製劑誘導的細胞死亡,但 CD38 有利於細胞死亡,而 CD73 通過分別將 NAD 和 NMN 降解為 NAM,將 NMN 降解為 NR 來維持細胞活力,從而維持 NAD+ 合成 . 在致癌小鼠模型中,補充 NMN(每天 500 mg/kg 體重,持續 13 天)顯著增加了與促炎性衰老相關的分泌表型,促進了胰腺導管腺癌的進展。 這就提出了一個假設,即膳食補充劑可以增加 NAD+,並且在壓力條件下可能在體內致瘤,例如由激活的癌基因誘導的癌前衰老病變。
因此,值得考慮 NAD+ 依賴過程之間複雜的相互作用和調節的程度。
一項針對大鼠的毒性研究表明,在亞慢性(90 天)治療期內以高達 1500 mg/kg/天的劑量重複口服合成 NMN (NMN-C®) 似乎是安全的,並且不會促進毒性 從體重變化、食物和水消耗、飼料轉化效率、生化和血液參數中可以看出效果 ,儘管在中高劑量(750 mg/kg)的動物中發現了幾個生理和生化參數的差異 /天和 1500 mg/kg/天)。 與對照相比,腎臟、肝臟和腎上腺的重量有所增加,這與腎臟和肝臟的組織病理學發現相關。 相應地,發現肝酶鹼性磷酸酶、丙氨酸氨基轉移酶和天冬氨酸氨基轉移酶水平升高。 因此,對於一個 60 公斤的人來說,確定的 NMN 攝入量上限為每天 900 毫克。
第一項臨床試驗報告稱,單次口服 NMN(100 至 500 毫克)可在健康受試者中安全有效地代謝。 它顯示血漿中代謝物以劑量依賴的方式顯著增加,而不會引起不良反應或任何顯著的臨床症狀或心率、血壓、氧飽和度和體溫的變化。 然而,在血漿中未檢測到 NMN,很可能是因為樣品在提取前冷凍可能導致 NMN 降解。 據報導,NMN 在−80 °C 時在血液中降解非常迅速。
在健康受試者中,NMN(250 毫克/天,持續 12 週)可提高全血中的 NAD+ 水平,且無明顯不良反應,未觀察到生理和臨床實驗室檢查異常。 另一項涉及 40 至 65 歲健康受試者的研究發現,口服 NMN 補充劑 (300 毫克) 60 天也具有良好的耐受性,沒有觀察到有害影響。 儘管 NMN 和安慰劑組之間的差異無統計學意義,但血清中的 NAD+ /NADH 水平增加了 38%(從基線的 6.57 pmol/ml 增加到研究結束時的 9.07 pmol/ml)。
口服 NMN 在小鼠組織中迅速合成為 NAD+ 。 口服強飼法(300 毫克/千克體重)後,NMN 迅速從腸道吸收到血液中,並在 15 分鐘內從循環中消除,在 15 至 30 分鐘時肝臟 NAD+ 水平持續升高。 這表明由於 NMN 從血漿到組織的平衡分佈,血漿 NMN 水平也可能保持較低和恆定。
口服 NR 增加 NAD+ 濃度 > 兩倍(NR 47.75 μM 與安慰劑 20.90 μM),NAAD 增加 4.5 倍,NMN 增加 1.4 倍,而不會導致血液中的 NAM 增加。 NR 後 NAM 去除途徑非常活躍,MeNAM、Me-2py 和 Me-4py 過量,尿液中 NAR 增加約 20 倍 。
馬滕斯等人。 (2018) 發現補充 NR(1 克/天)6 週的健康中年男性和女性血液中的 NAAD 水平增加了約五倍。 在另一項研究中,在使用前未在人體血液中檢測到 NAAD NR 補充劑,而健康個體服用單劑量高達 1 g NR(100、300 和 1000 mg)的 NAAD 基線增加了約 2,900%。 因此,證實 NAAD 是人類利用 NR 的產物,也是 NAD+ 代謝增加的生物標誌物,這證實了小鼠的發現,即代謝 NR 脫酰胺 Preiss-Handler 途徑占主導地位。
NMN 對骨骼肌生物學產生顯著影響,與安慰劑組相比,血小板衍生生長因子結合途徑的差異表達基因顯著增加 。 儘管肌肉 NAD+ 含量在 10 週後沒有變化,但 NMN 治療增加了肌肉代謝物 N1-甲基煙酰胺 (MeNAM)、N1-甲基-2-吡啶酮-5-甲酰胺 (Me-2py) 和 N1-甲基-4-吡啶酮-5 -甲酰胺 (Me-4py)。 入江等。 還觀察到口服 NMN 補充劑後這些代謝物的增加,表明 NMN 增加了肌肉 NAD+ 的轉換。
NMN和NR的預防和治療作用
例如,NAMPT 抑制導致的 NAD 合成抑制會降低細胞生長並增加對氧化應激的易感性,這已成為癌症治療的一個治療概念。 雖然 NAD+ 前體 NMN 和 NR 可逆轉 NAMPT 抑製劑誘導的細胞死亡,但 CD38 有利於細胞死亡,而 CD73 通過分別將 NAD 和 NMN 降解為 NAM,將 NMN 降解為 NR 來維持細胞活力,從而維持 NAD+ 合成 . 在致癌小鼠模型中,補充 NMN(每天 500 mg/kg 體重,持續 13 天)顯著增加了與促炎性衰老相關的分泌表型,促進了胰腺導管腺癌的進展。 這就提出了一個假設,即膳食補充劑可以增加 NAD+,並且在壓力條件下可能在體內致瘤,例如由激活的癌基因誘導的癌前衰老病變。
因此,值得考慮 NAD+ 依賴過程之間複雜的相互作用和調節的程度。
一項針對大鼠的毒性研究表明,在亞慢性(90 天)治療期內以高達 1500 mg/kg/天的劑量重複口服合成 NMN (NMN-C®) 似乎是安全的,並且不會促進毒性 從體重變化、食物和水消耗、飼料轉化效率、生化和血液參數中可以看出效果 ,儘管在中高劑量(750 mg/kg)的動物中發現了幾個生理和生化參數的差異 /天和 1500 mg/kg/天)。 與對照相比,腎臟、肝臟和腎上腺的重量有所增加,這與腎臟和肝臟的組織病理學發現相關。 相應地,發現肝酶鹼性磷酸酶、丙氨酸氨基轉移酶和天冬氨酸氨基轉移酶水平升高。 因此,對於一個 60 公斤的人來說,確定的 NMN 攝入量上限為每天 900 毫克。
第一項臨床試驗報告稱,單次口服 NMN(100 至 500 毫克)可在健康受試者中安全有效地代謝。 它顯示血漿中代謝物以劑量依賴的方式顯著增加,而不會引起不良反應或任何顯著的臨床症狀或心率、血壓、氧飽和度和體溫的變化。 然而,在血漿中未檢測到 NMN,很可能是因為樣品在提取前冷凍可能導致 NMN 降解。 據報導,NMN 在−80 °C 時在血液中降解非常迅速。
在健康受試者中,NMN(250 毫克/天,持續 12 週)可提高全血中的 NAD+ 水平,且無明顯不良反應,未觀察到生理和臨床實驗室檢查異常。 另一項涉及 40 至 65 歲健康受試者的研究發現,口服 NMN 補充劑 (300 毫克) 60 天也具有良好的耐受性,沒有觀察到有害影響。 儘管 NMN 和安慰劑組之間的差異無統計學意義,但血清中的 NAD+ /NADH 水平增加了 38%(從基線的 6.57 pmol/ml 增加到研究結束時的 9.07 pmol/ml)。
口服 NMN 在小鼠組織中迅速合成為 NAD+ 。 口服強飼法(300 毫克/千克體重)後,NMN 迅速從腸道吸收到血液中,並在 15 分鐘內從循環中消除,在 15 至 30 分鐘時肝臟 NAD+ 水平持續升高。 這表明由於 NMN 從血漿到組織的平衡分佈,血漿 NMN 水平也可能保持較低和恆定。
口服 NR 增加 NAD+ 濃度 > 兩倍(NR 47.75 μM 與安慰劑 20.90 μM),NAAD 增加 4.5 倍,NMN 增加 1.4 倍,而不會導致血液中的 NAM 增加。 NR 後 NAM 去除途徑非常活躍,MeNAM、Me-2py 和 Me-4py 過量,尿液中 NAR 增加約 20 倍 。
馬滕斯等人。 (2018) 發現補充 NR(1 克/天)6 週的健康中年男性和女性血液中的 NAAD 水平增加了約五倍。 在另一項研究中,在使用前未在人體血液中檢測到 NAAD NR 補充劑,而健康個體服用單劑量高達 1 g NR(100、300 和 1000 mg)的 NAAD 基線增加了約 2,900%。 因此,證實 NAAD 是人類利用 NR 的產物,也是 NAD+ 代謝增加的生物標誌物,這證實了小鼠的發現,即代謝 NR 脫酰胺 Preiss-Handler 途徑占主導地位。
NMN 對骨骼肌生物學產生顯著影響,與安慰劑組相比,血小板衍生生長因子結合途徑的差異表達基因顯著增加 。 儘管肌肉 NAD+ 含量在 10 週後沒有變化,但 NMN 治療增加了肌肉代謝物 N1-甲基煙酰胺 (MeNAM)、N1-甲基-2-吡啶酮-5-甲酰胺 (Me-2py) 和 N1-甲基-4-吡啶酮-5 -甲酰胺 (Me-4py)。 入江等。 還觀察到口服 NMN 補充劑後這些代謝物的增加,表明 NMN 增加了肌肉 NAD+ 的轉換。
NMN和NR的預防和治療作用
從歷史上看,NAD 生物合成前體色氨酸、NA 和 NAM 已被用於預防和治療糙皮病,這是一種以黑色素皮疹為特徵的疾病,可引起所謂的 3D(皮炎、腹瀉和癡呆)。 單獨的色氨酸不足以維持 NAD+ 的細胞水平,因為它參與其他代謝途徑,例如血清素、褪黑激素和吡啶甲酸合成。 藥理劑量的 NA 可降低人體血清膽固醇水平; 然而,它的使用受到限制,因為其副作用會導致皮膚潮紅,並伴有令人不快的溫暖感,並且經常會發癢 。
儘管 NAM 已被證明可有效增加組織中的 NAD+,但它也對 sirtuin 和 PARP 活性 產生抑製作用。 在高劑量下,NAM 導致甲基化增加,通過煙酰胺 N-甲基轉移酶 (NNMT) 生成 N1-甲基煙酰胺 (MeNAM),以便在尿液中消除,隨著時間的推移,這會降低細胞甲基池。 一旦基因啟動子區域的 DNA 甲基化通常與轉錄抑制相關,這可能導致 DNA 和蛋白質甲基化的減少,並因此改變基因表達模式和蛋白質活性。
此外,在大鼠身上進行的血液和尿液藥代動力學數據表明,腹膜內給藥的 NMN 似乎比 NAM 在體內保留的時間更長 。 目前尚不清楚為什麼 NR 給藥比 NAM 和 NA 治療更能增加 NAD+水平,而 NMN 和 NAM 給藥顯示血液和肝臟中的 NAD 水平沒有差異。 在相同劑量下直接比較所有前體的進一步研究對於闡明每個前體的優勢目的很重要。
NMN 被提議作為預防與年齡相關的生理衰退的營養保健品,已證明可以改善糖尿病和阿爾茨海默氏病,增強有氧能力,並表現出 心臟和血管保護作用。 它可以抑制炎症並減少氧化應激,預防動脈和內皮功能障礙 ,並防止心力衰竭、缺血和再灌注。
NR 在阿爾茨海默病模型中顯示出對認知功能、突觸可塑性、學習、記憶和運動功能的保護作用。 它降低了 β-澱粉樣蛋白水平,使 NR 處理的 Tg2576 小鼠識別新物體的機會增加了 20%。 此外,NR 顯著減少了神經炎症、海馬神經元凋亡、磷酸化 Tau 和 DNA 損傷,同時還使神經發生增加了近 20% 。
此外,NR 已被證明可以預防和改善代謝紊亂,例如高脂飲食引起的肥胖和非酒精性脂肪肝 (NAFLD)。 它通過增加能量消耗來促進代謝靈活性,從而顯著減弱高脂肪飲食引起的體重增加和脂肪量減少,特別是在肝臟中,甘油三酯水平降低了 40% 。 NR 增加肝臟 β-氧化和線粒體含量,從而逆轉葡萄糖耐受不良、胰島素抵抗、肝臟脂質積累和肝纖維化 。
儘管它可能還有其他尚未闡明的機制,但 NMN 和 NR 的有益作用主要歸因於增加 NAD+ 水平,從而使 sirtuins 活動及其潛在目標成為可能。
抗衰老作用
將衰老歸類為一種疾病或一種自然而普遍的過程被認為是有爭議的; 然而,眾所周知,細胞功能下降是衰老過程的一部分。
人們認識到,隨著衰老,各種組織中 NAD+ 水平的降低在多種疾病的病理生理學中起著關鍵作用,包括與年齡相關的代謝紊亂、神經退行性疾病和精神障礙 . 這種與年齡相關的 NAD+下降的一個重要原因是 NAMPT 介導的生物合成減少。 器官中的 NAMPT(煙酰胺磷酸核糖基轉移酶)蛋白和 NAD+ 水平顯著降低,例如老年小鼠的白色脂肪組織和骨骼肌,影響 NAD+ 依賴性酶(如 sirtuins)的活性 。 結果,影響細胞內氧化還原反應的平衡,導致功能下降。
另一個導致 NAD+ 水平低的原因是胞外酶 CD38。 CD38 的水平和活性隨著年齡的增長而增加,並且是 NAD 下降和線粒體功能障礙所必需的 。 還發現 CD38 降解 NMN,從而改變 NMN 和 NR 的藥代動力學。 因此,CD38 調節 NAD+、NMN 的水平,此外還調節 SIRT1 活性,在與年齡相關的疾病的發作中發揮關鍵作用。 事實上,CD38 是調節神經變性的候選分子。 小鼠中的 CD38 敲低抑制了軸突變性、脫髓鞘和免疫細胞浸潤與野生型小鼠相比,面神經軸索切斷術後的定量。 相應地,在面神經軸索切斷術、延遲軸突變性和脫髓鞘之前每天一次腹腔注射 NR (400 mg/kg),持續 1 週,顯著增加野生型小鼠的面神經核和麵神經 NAD+水平。
在衰老過程中,DNA 損傷在細胞核中累積,導致 PARP 激活並降低 NAD+ 水平和 SIRT1 活性。 SIRT1 是一種去乙酰化酶 (SIRT1-7),它使用 NAD+ 作為底物催化蛋白質的脫乙酰化或單-ADP-核糖基化反應。 此外,染色體區域累積的 DNA 損傷會導致染色體末端保護性端粒序列的逐漸累積丟失。 短端粒顯示 sirtuins 的表達和活性降低以及顯著的線粒體功能障礙。
NMN 促進老年小鼠、衰老前小鼠和人類的端粒延長。 用 NMN 處理(溶解在 5 毫米飲用水中 8 週)促進第 4 代 (G4) 小鼠的端粒延長,抑制 DNA 損傷反應和 p53,功能性挽救肝纖維化,並改善部分 SIRT1 中的線粒體生物發生和功能 -依賴的方式。 NMN 處理的 G4 小鼠肝組織中 NAD+ 水平的增加逆轉了幾個 sirtuin 靶標的過度乙酰化,表明 sirtuin 活性得到加強 。 SIRT1 通過去乙酰化和激活 PGC1α(過氧化物酶體增殖物激活受體-γ 共激活因子 1α)來增加線粒體活性和生物發生。 PGC1α 是線粒體基因的轉錄輔助調節劑,可以解毒消除 ROS(活性氧)的酶,從而改善新陳代謝和抗氧化保護。
線粒體是人體的重要細胞器,它從食物中產生細胞使用的大部分能量。 幾乎所有的代謝過程都依賴於 NAD+,因此,線粒體 NAD+ 水平的維持對於細胞存活至關重要。 隨著年齡的增長,線粒體變得越來越功能失調,線粒體自噬和生物能量能力有缺陷,最終會在細胞內產生過量的自由基,從而破壞全球細胞環境。 長期服用 NMN(在 100 或 300 mg/kg/天的飲用水中隨意服用,持續 12 個月增加了骨骼肌中的線粒體呼吸能力,並以組織特異性方式逆轉了與年齡相關的基因表達變化 。 此外,口服的 NMN 被迅速吸收,進入血液循環,並立即在肝臟和比目魚肌等主要代謝組織中轉化為 NAD+ ,改善能量消耗、耗氧量、胰島素敏感性、血漿脂質譜、眼功能、 老年小鼠的骨密度和骨髓-淋巴細胞組成。
表 1 總結了 NR 和 NMN 補充劑的其他動物和人體研究,包括抗衰老作用。
儘管 NAM 已被證明可有效增加組織中的 NAD+,但它也對 sirtuin 和 PARP 活性 產生抑製作用。 在高劑量下,NAM 導致甲基化增加,通過煙酰胺 N-甲基轉移酶 (NNMT) 生成 N1-甲基煙酰胺 (MeNAM),以便在尿液中消除,隨著時間的推移,這會降低細胞甲基池。 一旦基因啟動子區域的 DNA 甲基化通常與轉錄抑制相關,這可能導致 DNA 和蛋白質甲基化的減少,並因此改變基因表達模式和蛋白質活性。
此外,在大鼠身上進行的血液和尿液藥代動力學數據表明,腹膜內給藥的 NMN 似乎比 NAM 在體內保留的時間更長 。 目前尚不清楚為什麼 NR 給藥比 NAM 和 NA 治療更能增加 NAD+水平,而 NMN 和 NAM 給藥顯示血液和肝臟中的 NAD 水平沒有差異。 在相同劑量下直接比較所有前體的進一步研究對於闡明每個前體的優勢目的很重要。
NMN 被提議作為預防與年齡相關的生理衰退的營養保健品,已證明可以改善糖尿病和阿爾茨海默氏病,增強有氧能力,並表現出 心臟和血管保護作用。 它可以抑制炎症並減少氧化應激,預防動脈和內皮功能障礙 ,並防止心力衰竭、缺血和再灌注。
NR 在阿爾茨海默病模型中顯示出對認知功能、突觸可塑性、學習、記憶和運動功能的保護作用。 它降低了 β-澱粉樣蛋白水平,使 NR 處理的 Tg2576 小鼠識別新物體的機會增加了 20%。 此外,NR 顯著減少了神經炎症、海馬神經元凋亡、磷酸化 Tau 和 DNA 損傷,同時還使神經發生增加了近 20% 。
此外,NR 已被證明可以預防和改善代謝紊亂,例如高脂飲食引起的肥胖和非酒精性脂肪肝 (NAFLD)。 它通過增加能量消耗來促進代謝靈活性,從而顯著減弱高脂肪飲食引起的體重增加和脂肪量減少,特別是在肝臟中,甘油三酯水平降低了 40% 。 NR 增加肝臟 β-氧化和線粒體含量,從而逆轉葡萄糖耐受不良、胰島素抵抗、肝臟脂質積累和肝纖維化 。
儘管它可能還有其他尚未闡明的機制,但 NMN 和 NR 的有益作用主要歸因於增加 NAD+ 水平,從而使 sirtuins 活動及其潛在目標成為可能。
抗衰老作用
將衰老歸類為一種疾病或一種自然而普遍的過程被認為是有爭議的; 然而,眾所周知,細胞功能下降是衰老過程的一部分。
人們認識到,隨著衰老,各種組織中 NAD+ 水平的降低在多種疾病的病理生理學中起著關鍵作用,包括與年齡相關的代謝紊亂、神經退行性疾病和精神障礙 . 這種與年齡相關的 NAD+下降的一個重要原因是 NAMPT 介導的生物合成減少。 器官中的 NAMPT(煙酰胺磷酸核糖基轉移酶)蛋白和 NAD+ 水平顯著降低,例如老年小鼠的白色脂肪組織和骨骼肌,影響 NAD+ 依賴性酶(如 sirtuins)的活性 。 結果,影響細胞內氧化還原反應的平衡,導致功能下降。
另一個導致 NAD+ 水平低的原因是胞外酶 CD38。 CD38 的水平和活性隨著年齡的增長而增加,並且是 NAD 下降和線粒體功能障礙所必需的 。 還發現 CD38 降解 NMN,從而改變 NMN 和 NR 的藥代動力學。 因此,CD38 調節 NAD+、NMN 的水平,此外還調節 SIRT1 活性,在與年齡相關的疾病的發作中發揮關鍵作用。 事實上,CD38 是調節神經變性的候選分子。 小鼠中的 CD38 敲低抑制了軸突變性、脫髓鞘和免疫細胞浸潤與野生型小鼠相比,面神經軸索切斷術後的定量。 相應地,在面神經軸索切斷術、延遲軸突變性和脫髓鞘之前每天一次腹腔注射 NR (400 mg/kg),持續 1 週,顯著增加野生型小鼠的面神經核和麵神經 NAD+水平。
在衰老過程中,DNA 損傷在細胞核中累積,導致 PARP 激活並降低 NAD+ 水平和 SIRT1 活性。 SIRT1 是一種去乙酰化酶 (SIRT1-7),它使用 NAD+ 作為底物催化蛋白質的脫乙酰化或單-ADP-核糖基化反應。 此外,染色體區域累積的 DNA 損傷會導致染色體末端保護性端粒序列的逐漸累積丟失。 短端粒顯示 sirtuins 的表達和活性降低以及顯著的線粒體功能障礙。
NMN 促進老年小鼠、衰老前小鼠和人類的端粒延長。 用 NMN 處理(溶解在 5 毫米飲用水中 8 週)促進第 4 代 (G4) 小鼠的端粒延長,抑制 DNA 損傷反應和 p53,功能性挽救肝纖維化,並改善部分 SIRT1 中的線粒體生物發生和功能 -依賴的方式。 NMN 處理的 G4 小鼠肝組織中 NAD+ 水平的增加逆轉了幾個 sirtuin 靶標的過度乙酰化,表明 sirtuin 活性得到加強 。 SIRT1 通過去乙酰化和激活 PGC1α(過氧化物酶體增殖物激活受體-γ 共激活因子 1α)來增加線粒體活性和生物發生。 PGC1α 是線粒體基因的轉錄輔助調節劑,可以解毒消除 ROS(活性氧)的酶,從而改善新陳代謝和抗氧化保護。
線粒體是人體的重要細胞器,它從食物中產生細胞使用的大部分能量。 幾乎所有的代謝過程都依賴於 NAD+,因此,線粒體 NAD+ 水平的維持對於細胞存活至關重要。 隨著年齡的增長,線粒體變得越來越功能失調,線粒體自噬和生物能量能力有缺陷,最終會在細胞內產生過量的自由基,從而破壞全球細胞環境。 長期服用 NMN(在 100 或 300 mg/kg/天的飲用水中隨意服用,持續 12 個月增加了骨骼肌中的線粒體呼吸能力,並以組織特異性方式逆轉了與年齡相關的基因表達變化 。 此外,口服的 NMN 被迅速吸收,進入血液循環,並立即在肝臟和比目魚肌等主要代謝組織中轉化為 NAD+ ,改善能量消耗、耗氧量、胰島素敏感性、血漿脂質譜、眼功能、 老年小鼠的骨密度和骨髓-淋巴細胞組成。
表 1 總結了 NR 和 NMN 補充劑的其他動物和人體研究,包括抗衰老作用。
抗 COVID-19 作用
年齡也是 COVID-19 患者的一個危險因素,增加了患重病和死亡的機率。 原因是衰老過程會導致一些變化,尤其是會損害免疫反應的免疫衰老和炎症。 端粒縮短和幼稚淋巴細胞減少導致免疫功能受損和循環促炎細胞因子升高是導致 COVID-19 病例惡化的因素 。
有證據表明 NAD+在調節 COVID-19 疾病結果(大流行性公共衛生爆發)方面的潛在相關性。 在 SARS-CoV-2 感染期間,與 NAD+ 合成和使用相關的一組基因失調 ,這可能是由於對 NAD+ 代謝途徑的需求增加所致。
已知 PARP 在抑制病毒基因組中通過 ADP-核糖基化轉錄本的翻譯方面發揮關鍵的抗病毒作用,需要 NAD+。 然而,包括 SARS-CoV 在內的幾個病毒家族編碼一種宏結構域蛋白,該蛋白水解蛋白質和核酸的 ADPR 單元,抑制 PARP 的保護作用,然後促進複製和毒力。 因此,PARP 的過度激活會補償 ADPR 的水解,同時伴隨著 NAD+ 的消耗,這表明增加 NAD+ 水平可能會恢復 PARP 的抗病毒功能,以支持對 SARS-CoV-2 的免疫力 。
除了 PARPS 對免疫反應的作用外,sirtuins 還可以協調炎症反應的強度,防止細胞因子風暴的影響。 SIRT1、SIRT2 和 SIRT3 均通過多種機制抑制 NF-κB(核因子 kappa B)和 NLRP3(Nod 樣受體家族蛋白 3)炎性體的活性。 SIRT6 通過 NF-κB 靶基因啟動子染色質上的組蛋白 H3 賴氨酸 9 (H3K9) 脫乙酰化減弱 NF-κB 信號,這與細胞凋亡和細胞衰老有關。
在一項對 10 名 50 歲以上重症患者的案例研究中,NMN 雞尾酒(83 mL NMN 與 400 mL 水混合,早餐和晚餐前食用)與 COVID-19 症狀緩解密切相關。 治療前,患者存在低氧飽和度、肺部浸潤和炎症。 治療後,雙側肺部浸潤、發熱消退和炎症生物標誌物均有快速改善。 然而,一名患者因溝通不暢而在 3 天后停止治療,並在 8 天后出現發熱和肺部浸潤復發。 快速有效的臨床改善表明 NMN 可能在逆轉 SARS-CoV-2 感染引發的潛在致命細胞因子風暴中發揮作用。
一項研究表明,由 NR(1 克)、左旋肉鹼酒石酸鹽(3.73 克)、N-乙酰半胱氨酸(2.55 克)和絲氨酸(12.35 克)組成的聯合代謝激活劑 (CMA) 改善了 COVID-19 的結果。 患者在早上早餐後口服一劑混合物,晚餐後口服一劑,持續 14 天。 在安慰劑對照、開放標籤的 2 期研究和雙盲 3 期臨床試驗中,與安慰劑組相比,服用 CMA 的患者的完全康復時間明顯更快(分別為 6.6 天和 9.3 天以及 5.7 天和 9.2 天)。 發現 CMA 可增強免疫反應並調節氨基酸和脂質代謝。 此外,接受 CMA 治療的患者血漿中幾種炎症和抗氧化代謝相關生物標誌物的水平顯著改善,例如丙氨酸轉氨酶 (ALT)、乳酸脫氫酶 (LDH)、肌酐、葡萄糖和蛋白質。
研究發現,嘌呤代謝的改變會導致 COVID-19 期間的免疫失調,可能導致疾病的嚴重程度。 與健康對照組相比,未接種疫苗的重症 COVID-19 患者血漿中的 ATP 水平更高,腺苷水平更低。 負責 ATP 裂解成腺苷的外核苷酸酶 CD39 和 CD73 在重症 COVID-19 患者血液中的表達降低。 除了 ATP 的生成受損外,腺苷受體的表達也較少,以疾病嚴重程度依賴的方式。 由於腺苷及其受體作用於中性粒細胞和單核細胞/巨噬細胞,抑制細胞因子的產生,不平衡的 ATP/腺苷比例會干擾這種抗炎調節。 此外,體外給予外源性腺苷可預防患者白細胞的炎症反應,這種 ATP 代謝改變是否是對 SARS-CoV-2 炎症反應加劇的原因或影響仍有待探索 . 鑑於 NAD+ 在 ATP 生成中的功能以及細胞外 NAD+ 和 ATP 在調節炎症和免疫反應中的作用,值得研究 NAD+ 可能參與 SARS-CoV 感染期間這種改變的 ATP 代謝-2。
抗炎作用
增加 NAD+ 可以減少炎症。 與 NR 在增加 NAD+ 水平和隨後的 SIRT3 激活中的已知作用一致,對來自健康受試者的 PBMCs 的 24 小時 NR(未描述的量)給藥複製了鈍化 NLRP3 炎性體激活和通過 SIRT3 增強線粒體質量控制的禁食效果 NR 減少 SOD2 和異檸檬酸脫氫酶 2 的乙酰化,同時增加線粒體 SOD2 活性,從而降低線粒體 ROS 水平。 此外,NR 減少了健康志願者單核細胞和巨噬細胞中白介素-1β (IL-1β) 和腫瘤壞死因子-α (TNF-α) 的分泌,IL-1β 的單核細胞減少超過 50%(從大約 22,000 至 10,000 pg/mL)和超過 75% 的 TNF-α(從高於 2000 到低於 500 pg/mL)。
在老年男性中,連續 3 週每天補充 1 克口服 NR 會增加全血和骨骼肌中的 NAD+> 代謝組水平,並顯著降低炎症細胞因子 IL-2、IL-5、IL-6 和 TNF-的循環水平 α 與基線相比(白介素約為 20 至 5 pg/ml,TNF-α 約為 250 至 200 pg/ml)。
除了增加細胞 NAD+ 水平降低外,NMN (500 μM) 處理還減少了 LPS 激活的小鼠和人巨噬細胞系(THP-1、RAW264.7)中促炎細胞因子的產生。 NMN 通過 COX-2-PGE2 軸和抑制炎症相關通路有效減輕 LPS 誘導的炎症和氧化應激。 蛋白質組學分析發現,NMN 下調環氧合酶 2 (COX-2) 的表達,並顯著降低 IL-6 和 IL-1β 的 mRNA 表達和細胞外分泌,以及前列腺素 E2 (PGE2) 的細胞水平。 與 LPS 處理的細胞相比,LPS/NMN 共同處理的細胞中與炎症反應相關的蛋白質,如 RELL1、PTGS2、FGA、FGB 和 igkv12-44 均有所減少。 NMN 治療還抑制其他炎症相關通路,如前列腺素生物合成、LPS/IL-1 介導的 RXR 功能抑制、IL-6 信號和 NF-κB 信號。
能量代謝的調節
NAD+在主要能量生產途徑的各種氧化還原反應中充當輔酶,例如糖酵解、三羧酸 (TCA) 循環和脂肪酸氧化。 NAD+ 水平下降是能量穩態失衡的標誌,這使其成為一種能量感應代謝物。 能量感應通路對於維持能量生產和消耗之間的適當平衡很重要。 這些通路的紊亂會導致各種代謝紊亂,例如胰島素抵抗和脂肪肝。
在營養不良的情況下,例如高脂肪和高蛋白質攝入,NAD+水平會降低。 當消耗過多的卡路里時,低 AMP/ATP 比率會導致 NAD+ 或 NAD+⟩/NADH 比率降低。 腺苷一磷酸激活蛋白激酶 (AMPK) 是一種細胞能量調節劑,可感知細胞內 AMP/ATP 比率的變化。 在能量限制期間,低水平的 ATP 會激活 AMPK,後者起到維持細胞能量儲存的作用。 AMPK 開啟產生 ATP 的分解代謝途徑,主要是通過增強氧化代謝和線粒體生物合成,同時關閉消耗 ATP 的合成代謝途徑,從而改變 NAD+ /NADH 比率。 因此,AMPK 通過增加細胞 NAD+ 水平來增強 SIRT1 活性,從而導致能量代謝相關下游 SIRT1 靶標的去乙酰化和活性調節,其中包括 PGC1α、叉頭盒 O1 (FOXO1) 和 O3 (FOXO3a) 轉錄因子 。
相應地,施用 NR 或 NMN 可以防止 NAD 水平降低。 NR(450 mg/kg 體重,持續 45 天)穩定心肌 NAD+ 水平,增加糖酵解以及檸檬酸鹽和乙酰輔酶 A 代謝,減輕擴張型心肌病小鼠模型心力衰竭的發展 。 通過增加小鼠肝臟和肌肉中的 NAD+水平,NR 補充劑(400 mg/kg/天)刺激 SIRT1 和 SIRT3 活性,增強線粒體功能、氧化代謝、能量消耗和耐力表現。 此外,NR 可以防止高脂肪飲食的有害代謝影響,包括高胰島素血症、總膽固醇和低密度脂蛋白膽固醇水平升高以及體重增加,儘管在正常飲食中服用 NR 對體重沒有影響.
NMN 還證明對進食食物的小鼠的葡萄糖代謝沒有有益作用。 將斷奶後 30 週餵食普通食物或高脂肪飲食 (HFD) 的瘦和肥胖祖母小鼠的雄性後代腹膜內註射 NMN(500 毫克/千克體重)持續 21 天。 這些小鼠的肥胖、肝臟和血漿甘油三酯水平降低。 此外,在攝入 HFD 的後代中,參與脂肪合成、運輸和攝取的肝臟基因減少,而參與脂肪酸氧化的基因因 NMN 而增加。 然而,就葡萄糖耐量而言,NMN 僅對代謝受損最嚴重的小鼠組(餵食 HFD 和來自肥胖的母鼠)有益。 此外,NMN 會損害來自食用食物的瘦後代小鼠的葡萄糖耐量,並且對食用 HFD 的後代沒有額外影響。 在另一項研究中,NMN 補充劑(400 mg/kg,持續 8 週)降低了肥胖小鼠運動誘導的益處,例如肝甘油三酯積累減少、葡萄糖刺激的胰島胰島素分泌和葡萄糖耐量。 儘管 NMN 自身顯著下調胰島中 TNF-α 和 Tlr4 的表達並上調 PGC-1α 的表達以支持其抗氧化作用,但 NMN 與運動的結合提高了抗氧化劑與促氧化劑的比例,解除了對氧化還原穩態的調節。
這些結果表明,在 NAD+ 水平平衡的情況下,補充 NAD+ 前體可能效果較差。
抗糖尿病作用
糖尿病的標誌性高血糖會導致 NAD+ 和 NADH 比率之間的氧化還原失衡,從而導致氧化應激和多種代謝綜合徵。 對於葡萄糖攝取不依賴於胰島素的細胞,葡萄糖供應過剩會導致傳統葡萄糖燃燒途徑(糖酵解和克雷布斯循環)和多元醇途徑產生 NADH 過量。 這種 NAD+ /NADH 比例失衡,也稱為假性缺氧,最初會導致還原應激、線粒體過載和功能障礙,從而導致氧化應激和大分子(包括 DNA、脂質和蛋白質)的氧化損傷。 另一方面,使用 NAD+ 作為 DNA 修復底物的 PARP 過度激活會減少或耗盡 NAD+。 因此,氧化還原失衡可能是導致糖尿病並發症發生的主要因素。
此外,這種以假性缺氧為特徵的氧化還原變化會激活兩條通路:甘油二酯 (DAG)–蛋白激酶 C (PKC) 和 (DAG)–蛋白激酶 D (PKD) 級聯,這會削弱 AMPK 活性,從而降低 NAD+ 的合成。 另一個建議可能是戊糖磷酸途徑的磷酸核糖基焦磷酸 (PPRP) 合成不足,糖尿病患者血漿硫胺素和蛋白激酶 B 活性降低會影響該途徑。 蛋白激酶 B 負責磷酸化和激活轉酮醇酶以產生 PPRP,後者將用於 NAD+ 通路合成。
NAD+含量降低和線粒體動力學失衡發生在糖尿病性心肌病的發展過程中。 每天口服強飼 NR 400 mg/kg/天,持續 4 周可減輕糖尿病引起的心肌病,改善糖尿病小鼠的心功能。 NR 升高心肌 NAD+ 含量並促進 mitofusin 2 介導的線粒體融合,通過 SIRT1-PGC1α-PPARα 途徑抑制氧化應激和細胞凋亡。
已知長期果糖餵養會抑制 eNAMPT 分泌和促炎細胞因子介導的胰島功能障礙,從而導致 β 細胞功能受損和血糖升高。 在這種情況下,NMN 給藥 (100 μmol/l) 以部分 SIRT1 依賴性方式恢復了用促炎細胞因子 IL1β 和 TNFα 培養的胰島中的胰島素分泌。 此外,它還糾正了炎症引起的胰島功能障礙,逆轉了編碼葡萄糖傳感和 β 細胞分化所必需的胰島標記基因表達的變化。 此外,通過改善餵食富含果糖飲食的小鼠的葡萄糖刺激的胰島素分泌,NMN(在組織取樣前 16 小時腹膜內給藥 500 mg/kg 體重)可能表明能夠通過抗炎症機制。
在另一項研究中,NMN 被證明是治療 2 型糖尿病病理生理學的有效干預措施。 在飲食和年齡誘導的糖尿病模型中,通過腹膜內註射 NMN(500 mg/kg 體重/天,持續 11 天)可顯著改善葡萄糖耐量受損並增強肝臟胰島素敏感性。 與氧化應激、炎症反應和晝夜節律相關的基因表達的指示逆轉變化部分是 SIRT1 激活的結果。 BESTO(β 細胞特異性 SIRT1 過表達)轉基因小鼠在高齡時失去了葡萄糖刺激的胰島素分泌表型,並且與年輕時一樣改善了葡萄糖耐量,儘管 SIRT1 在胰腺 β 細胞中保持過表達。 NMN 處理(進行測定前 14 小時 500 mg/kg 體重),此外增加了隨年齡增長而降低的 NAD+ 水平,能夠恢復老年 BESTO 小鼠的表型,並且還改善了老年野生型小鼠的葡萄糖刺激的胰島素分泌。
鑑於包括糖尿病在內的代謝疾病的多因素性質,NAD+前體有助於改善胰島素敏感性和血糖控制的機制可歸因於 NAD+ 水平的替代和/或增加以及氧化應激和炎症的逆轉。
在超重或肥胖和糖尿病前期的絕經後婦女中,口服 NMN 補充劑(每天 250 毫克,持續 10 週)可增加外周血單核細胞 (PBMC) 中的 NAD+含量,並改善骨骼肌中的胰島素信號傳導和敏感性 。
腸道菌群與 NAD+在宿主健康中的相互作用
年齡也是 COVID-19 患者的一個危險因素,增加了患重病和死亡的機率。 原因是衰老過程會導致一些變化,尤其是會損害免疫反應的免疫衰老和炎症。 端粒縮短和幼稚淋巴細胞減少導致免疫功能受損和循環促炎細胞因子升高是導致 COVID-19 病例惡化的因素 。
有證據表明 NAD+在調節 COVID-19 疾病結果(大流行性公共衛生爆發)方面的潛在相關性。 在 SARS-CoV-2 感染期間,與 NAD+ 合成和使用相關的一組基因失調 ,這可能是由於對 NAD+ 代謝途徑的需求增加所致。
已知 PARP 在抑制病毒基因組中通過 ADP-核糖基化轉錄本的翻譯方面發揮關鍵的抗病毒作用,需要 NAD+。 然而,包括 SARS-CoV 在內的幾個病毒家族編碼一種宏結構域蛋白,該蛋白水解蛋白質和核酸的 ADPR 單元,抑制 PARP 的保護作用,然後促進複製和毒力。 因此,PARP 的過度激活會補償 ADPR 的水解,同時伴隨著 NAD+ 的消耗,這表明增加 NAD+ 水平可能會恢復 PARP 的抗病毒功能,以支持對 SARS-CoV-2 的免疫力 。
除了 PARPS 對免疫反應的作用外,sirtuins 還可以協調炎症反應的強度,防止細胞因子風暴的影響。 SIRT1、SIRT2 和 SIRT3 均通過多種機制抑制 NF-κB(核因子 kappa B)和 NLRP3(Nod 樣受體家族蛋白 3)炎性體的活性。 SIRT6 通過 NF-κB 靶基因啟動子染色質上的組蛋白 H3 賴氨酸 9 (H3K9) 脫乙酰化減弱 NF-κB 信號,這與細胞凋亡和細胞衰老有關。
在一項對 10 名 50 歲以上重症患者的案例研究中,NMN 雞尾酒(83 mL NMN 與 400 mL 水混合,早餐和晚餐前食用)與 COVID-19 症狀緩解密切相關。 治療前,患者存在低氧飽和度、肺部浸潤和炎症。 治療後,雙側肺部浸潤、發熱消退和炎症生物標誌物均有快速改善。 然而,一名患者因溝通不暢而在 3 天后停止治療,並在 8 天后出現發熱和肺部浸潤復發。 快速有效的臨床改善表明 NMN 可能在逆轉 SARS-CoV-2 感染引發的潛在致命細胞因子風暴中發揮作用。
一項研究表明,由 NR(1 克)、左旋肉鹼酒石酸鹽(3.73 克)、N-乙酰半胱氨酸(2.55 克)和絲氨酸(12.35 克)組成的聯合代謝激活劑 (CMA) 改善了 COVID-19 的結果。 患者在早上早餐後口服一劑混合物,晚餐後口服一劑,持續 14 天。 在安慰劑對照、開放標籤的 2 期研究和雙盲 3 期臨床試驗中,與安慰劑組相比,服用 CMA 的患者的完全康復時間明顯更快(分別為 6.6 天和 9.3 天以及 5.7 天和 9.2 天)。 發現 CMA 可增強免疫反應並調節氨基酸和脂質代謝。 此外,接受 CMA 治療的患者血漿中幾種炎症和抗氧化代謝相關生物標誌物的水平顯著改善,例如丙氨酸轉氨酶 (ALT)、乳酸脫氫酶 (LDH)、肌酐、葡萄糖和蛋白質。
研究發現,嘌呤代謝的改變會導致 COVID-19 期間的免疫失調,可能導致疾病的嚴重程度。 與健康對照組相比,未接種疫苗的重症 COVID-19 患者血漿中的 ATP 水平更高,腺苷水平更低。 負責 ATP 裂解成腺苷的外核苷酸酶 CD39 和 CD73 在重症 COVID-19 患者血液中的表達降低。 除了 ATP 的生成受損外,腺苷受體的表達也較少,以疾病嚴重程度依賴的方式。 由於腺苷及其受體作用於中性粒細胞和單核細胞/巨噬細胞,抑制細胞因子的產生,不平衡的 ATP/腺苷比例會干擾這種抗炎調節。 此外,體外給予外源性腺苷可預防患者白細胞的炎症反應,這種 ATP 代謝改變是否是對 SARS-CoV-2 炎症反應加劇的原因或影響仍有待探索 . 鑑於 NAD+ 在 ATP 生成中的功能以及細胞外 NAD+ 和 ATP 在調節炎症和免疫反應中的作用,值得研究 NAD+ 可能參與 SARS-CoV 感染期間這種改變的 ATP 代謝-2。
抗炎作用
增加 NAD+ 可以減少炎症。 與 NR 在增加 NAD+ 水平和隨後的 SIRT3 激活中的已知作用一致,對來自健康受試者的 PBMCs 的 24 小時 NR(未描述的量)給藥複製了鈍化 NLRP3 炎性體激活和通過 SIRT3 增強線粒體質量控制的禁食效果 NR 減少 SOD2 和異檸檬酸脫氫酶 2 的乙酰化,同時增加線粒體 SOD2 活性,從而降低線粒體 ROS 水平。 此外,NR 減少了健康志願者單核細胞和巨噬細胞中白介素-1β (IL-1β) 和腫瘤壞死因子-α (TNF-α) 的分泌,IL-1β 的單核細胞減少超過 50%(從大約 22,000 至 10,000 pg/mL)和超過 75% 的 TNF-α(從高於 2000 到低於 500 pg/mL)。
在老年男性中,連續 3 週每天補充 1 克口服 NR 會增加全血和骨骼肌中的 NAD+> 代謝組水平,並顯著降低炎症細胞因子 IL-2、IL-5、IL-6 和 TNF-的循環水平 α 與基線相比(白介素約為 20 至 5 pg/ml,TNF-α 約為 250 至 200 pg/ml)。
除了增加細胞 NAD+ 水平降低外,NMN (500 μM) 處理還減少了 LPS 激活的小鼠和人巨噬細胞系(THP-1、RAW264.7)中促炎細胞因子的產生。 NMN 通過 COX-2-PGE2 軸和抑制炎症相關通路有效減輕 LPS 誘導的炎症和氧化應激。 蛋白質組學分析發現,NMN 下調環氧合酶 2 (COX-2) 的表達,並顯著降低 IL-6 和 IL-1β 的 mRNA 表達和細胞外分泌,以及前列腺素 E2 (PGE2) 的細胞水平。 與 LPS 處理的細胞相比,LPS/NMN 共同處理的細胞中與炎症反應相關的蛋白質,如 RELL1、PTGS2、FGA、FGB 和 igkv12-44 均有所減少。 NMN 治療還抑制其他炎症相關通路,如前列腺素生物合成、LPS/IL-1 介導的 RXR 功能抑制、IL-6 信號和 NF-κB 信號。
能量代謝的調節
NAD+在主要能量生產途徑的各種氧化還原反應中充當輔酶,例如糖酵解、三羧酸 (TCA) 循環和脂肪酸氧化。 NAD+ 水平下降是能量穩態失衡的標誌,這使其成為一種能量感應代謝物。 能量感應通路對於維持能量生產和消耗之間的適當平衡很重要。 這些通路的紊亂會導致各種代謝紊亂,例如胰島素抵抗和脂肪肝。
在營養不良的情況下,例如高脂肪和高蛋白質攝入,NAD+水平會降低。 當消耗過多的卡路里時,低 AMP/ATP 比率會導致 NAD+ 或 NAD+⟩/NADH 比率降低。 腺苷一磷酸激活蛋白激酶 (AMPK) 是一種細胞能量調節劑,可感知細胞內 AMP/ATP 比率的變化。 在能量限制期間,低水平的 ATP 會激活 AMPK,後者起到維持細胞能量儲存的作用。 AMPK 開啟產生 ATP 的分解代謝途徑,主要是通過增強氧化代謝和線粒體生物合成,同時關閉消耗 ATP 的合成代謝途徑,從而改變 NAD+ /NADH 比率。 因此,AMPK 通過增加細胞 NAD+ 水平來增強 SIRT1 活性,從而導致能量代謝相關下游 SIRT1 靶標的去乙酰化和活性調節,其中包括 PGC1α、叉頭盒 O1 (FOXO1) 和 O3 (FOXO3a) 轉錄因子 。
相應地,施用 NR 或 NMN 可以防止 NAD 水平降低。 NR(450 mg/kg 體重,持續 45 天)穩定心肌 NAD+ 水平,增加糖酵解以及檸檬酸鹽和乙酰輔酶 A 代謝,減輕擴張型心肌病小鼠模型心力衰竭的發展 。 通過增加小鼠肝臟和肌肉中的 NAD+水平,NR 補充劑(400 mg/kg/天)刺激 SIRT1 和 SIRT3 活性,增強線粒體功能、氧化代謝、能量消耗和耐力表現。 此外,NR 可以防止高脂肪飲食的有害代謝影響,包括高胰島素血症、總膽固醇和低密度脂蛋白膽固醇水平升高以及體重增加,儘管在正常飲食中服用 NR 對體重沒有影響.
NMN 還證明對進食食物的小鼠的葡萄糖代謝沒有有益作用。 將斷奶後 30 週餵食普通食物或高脂肪飲食 (HFD) 的瘦和肥胖祖母小鼠的雄性後代腹膜內註射 NMN(500 毫克/千克體重)持續 21 天。 這些小鼠的肥胖、肝臟和血漿甘油三酯水平降低。 此外,在攝入 HFD 的後代中,參與脂肪合成、運輸和攝取的肝臟基因減少,而參與脂肪酸氧化的基因因 NMN 而增加。 然而,就葡萄糖耐量而言,NMN 僅對代謝受損最嚴重的小鼠組(餵食 HFD 和來自肥胖的母鼠)有益。 此外,NMN 會損害來自食用食物的瘦後代小鼠的葡萄糖耐量,並且對食用 HFD 的後代沒有額外影響。 在另一項研究中,NMN 補充劑(400 mg/kg,持續 8 週)降低了肥胖小鼠運動誘導的益處,例如肝甘油三酯積累減少、葡萄糖刺激的胰島胰島素分泌和葡萄糖耐量。 儘管 NMN 自身顯著下調胰島中 TNF-α 和 Tlr4 的表達並上調 PGC-1α 的表達以支持其抗氧化作用,但 NMN 與運動的結合提高了抗氧化劑與促氧化劑的比例,解除了對氧化還原穩態的調節。
這些結果表明,在 NAD+ 水平平衡的情況下,補充 NAD+ 前體可能效果較差。
抗糖尿病作用
糖尿病的標誌性高血糖會導致 NAD+ 和 NADH 比率之間的氧化還原失衡,從而導致氧化應激和多種代謝綜合徵。 對於葡萄糖攝取不依賴於胰島素的細胞,葡萄糖供應過剩會導致傳統葡萄糖燃燒途徑(糖酵解和克雷布斯循環)和多元醇途徑產生 NADH 過量。 這種 NAD+ /NADH 比例失衡,也稱為假性缺氧,最初會導致還原應激、線粒體過載和功能障礙,從而導致氧化應激和大分子(包括 DNA、脂質和蛋白質)的氧化損傷。 另一方面,使用 NAD+ 作為 DNA 修復底物的 PARP 過度激活會減少或耗盡 NAD+。 因此,氧化還原失衡可能是導致糖尿病並發症發生的主要因素。
此外,這種以假性缺氧為特徵的氧化還原變化會激活兩條通路:甘油二酯 (DAG)–蛋白激酶 C (PKC) 和 (DAG)–蛋白激酶 D (PKD) 級聯,這會削弱 AMPK 活性,從而降低 NAD+ 的合成。 另一個建議可能是戊糖磷酸途徑的磷酸核糖基焦磷酸 (PPRP) 合成不足,糖尿病患者血漿硫胺素和蛋白激酶 B 活性降低會影響該途徑。 蛋白激酶 B 負責磷酸化和激活轉酮醇酶以產生 PPRP,後者將用於 NAD+ 通路合成。
NAD+含量降低和線粒體動力學失衡發生在糖尿病性心肌病的發展過程中。 每天口服強飼 NR 400 mg/kg/天,持續 4 周可減輕糖尿病引起的心肌病,改善糖尿病小鼠的心功能。 NR 升高心肌 NAD+ 含量並促進 mitofusin 2 介導的線粒體融合,通過 SIRT1-PGC1α-PPARα 途徑抑制氧化應激和細胞凋亡。
已知長期果糖餵養會抑制 eNAMPT 分泌和促炎細胞因子介導的胰島功能障礙,從而導致 β 細胞功能受損和血糖升高。 在這種情況下,NMN 給藥 (100 μmol/l) 以部分 SIRT1 依賴性方式恢復了用促炎細胞因子 IL1β 和 TNFα 培養的胰島中的胰島素分泌。 此外,它還糾正了炎症引起的胰島功能障礙,逆轉了編碼葡萄糖傳感和 β 細胞分化所必需的胰島標記基因表達的變化。 此外,通過改善餵食富含果糖飲食的小鼠的葡萄糖刺激的胰島素分泌,NMN(在組織取樣前 16 小時腹膜內給藥 500 mg/kg 體重)可能表明能夠通過抗炎症機制。
在另一項研究中,NMN 被證明是治療 2 型糖尿病病理生理學的有效干預措施。 在飲食和年齡誘導的糖尿病模型中,通過腹膜內註射 NMN(500 mg/kg 體重/天,持續 11 天)可顯著改善葡萄糖耐量受損並增強肝臟胰島素敏感性。 與氧化應激、炎症反應和晝夜節律相關的基因表達的指示逆轉變化部分是 SIRT1 激活的結果。 BESTO(β 細胞特異性 SIRT1 過表達)轉基因小鼠在高齡時失去了葡萄糖刺激的胰島素分泌表型,並且與年輕時一樣改善了葡萄糖耐量,儘管 SIRT1 在胰腺 β 細胞中保持過表達。 NMN 處理(進行測定前 14 小時 500 mg/kg 體重),此外增加了隨年齡增長而降低的 NAD+ 水平,能夠恢復老年 BESTO 小鼠的表型,並且還改善了老年野生型小鼠的葡萄糖刺激的胰島素分泌。
鑑於包括糖尿病在內的代謝疾病的多因素性質,NAD+前體有助於改善胰島素敏感性和血糖控制的機制可歸因於 NAD+ 水平的替代和/或增加以及氧化應激和炎症的逆轉。
在超重或肥胖和糖尿病前期的絕經後婦女中,口服 NMN 補充劑(每天 250 毫克,持續 10 週)可增加外周血單核細胞 (PBMC) 中的 NAD+含量,並改善骨骼肌中的胰島素信號傳導和敏感性 。
腸道菌群與 NAD+在宿主健康中的相互作用
我們回顧了有關 NAD+ 在維持細胞穩態中的核心功能的背景和最新發現。 眾所周知,腸道微生物群在宿主的代謝穩態、激素分泌和腦功能中的重要生理作用 。 同樣,腸道微生物與 NAD+ 代謝物之間的聯繫表明了有益生理效應的重要軸心。
一些腸道微生物可以產生對多種疾病具有保護作用的代謝物。 來自腸道微生物群的 NMN 通過增加 NAD+ 水平和激活 AP 小鼠模型中的 SIRT3-PRDX5 通路來改善急性胰腺炎 (AP) 損傷。 腸道菌群失調會加劇 AP,其特徵是有益微生物和致病微生物之間的失衡會增加腸道通透性、細菌易位和全身炎症反應。 除了恢復腸道菌群失調外,常生糞便菌群移植 (FMT) 還誘導了血清中更高水平的 NMN,從而增強了胰腺中 NAD+ 的生物合成。 與 FMT 類似,用 NMN 預處理(500 mg/kg 體重/天腹膜內給藥,連續 28 天)增加胰腺 NAD+ 水平,以部分 SIRT3 依賴的方式減輕 AP 介導的線粒體功能障礙、氧化損傷和炎症。 這些發現表明,NMN 是 FMT 在 AP 中的保護作用的重要介質,並強化了腸道微生物群對宿主 NAD+代謝和病理障礙結果的潛在作用。
除了腸道微生物群對 B 族維生素和 NAD+ 生物合成 的活性外,最近的證據表明 NAD+ 及其前體 NR 和 NMN 對腸道微生物群的調節作用,這可能是 觀察到的有益效果。 NAD+ 前體可以通過為有益細菌提供能量來源、激活sirtuins和改善腸道屏障功能來調節腸道微生物群。
NMN 和 NR 可以選擇性地刺激雙歧桿菌和乳酸桿菌等有益菌的生長 。 這些細菌與改善腸道健康有關,包括預防腹瀉、改善腸道屏障功能、減少炎症和支持免疫系統。 此外,NAD+ 前體對去乙酰化酶的激活也可能有助於對腸道微生物群和腸道健康產生有益影響。 Sirtuins 參與調節腸道微生物群和保護腸道內皮細胞免受氧化損傷 [130]。 最後,NMN 和 NR 還可以改善腸道屏障功能,這對於防止有害細菌和毒素從腸道轉移到血液中很重要。
除了改變組成和功能特徵外,NR 對腸道微生物群的調節被證明可以防止小鼠因高脂飲食 (HFD) 引起的體重增加 。 與補充有載體(水)的對照組相比,餵食 60% HFD 並補充 0.4% NR(168 天)的小鼠體重增加減少了近 16%,空腹血糖水平也降低了近 16%。 有趣的是,從 NR 處理的供體到餵食 HFD 的小鼠的糞便移植 (FMT) 也通過降低能量效率來減輕體重增加。 膳食 NR 補充劑和 FMT-NR 補充劑均導致腸道微生物組成發生改變,具有富含產丁酸鹽的厚壁菌門的獨特功能代謝特徵。 儘管一些厚壁菌門物種與肥胖有關,但厚壁菌門的許多物種具有益生菌和抗肥胖作用 。 例如,普氏梭菌、直腸真桿菌和羅氏桿菌產生短鏈脂肪酸,包括丁酸鹽,丁酸鹽已被證明可通過抑制腸道膽固醇生物合成和促進有益的代謝作用(例如胰島素分泌、胰島素敏感性和能量消耗)來減少肥胖 。 丁酸鹽還可以通過上調肽 YY 和胰高血糖素樣肽-1 (GLP-1) 的表達來增加飽腹感和腸道流動性。 此外,FMT-NR 小鼠的盲腸內容物中 NADH 水平顯著增加,表明盲腸中的微生物代謝發生了改變。
而確實NAD+可以直接影響腸道微生物的代謝。 由於 NAD+ 是所有生物體能量代謝的重要組成部分,主要是許多參與細胞 ATP 產生的關鍵酶的輔助因子,因此增加 NAD+ 可能會促進微生物的能量生產。 此外,NAD+可以通過關鍵的抑制性神經遞質 β-NAD 調節結腸的運動,並通過影響宿主膽汁酸的合成來間接影響腸道微生物,當它們破壞細菌細胞膜時可以發揮抗菌作用給小鼠膳食補充 NR 10 週(每天 400 mg/kg)可降低促炎和抗炎細胞因子水平,抑制小膠質細胞活化,並防止酒精引起的抑鬱樣行為。 這種效應歸因於 NR 通過改變腸道微生物群組成來上調腦源性神經營養因子 (BDNF) 的能力。 與對照組和 NR 組相比,酒精引起的抑鬱症小鼠模型在腸道微生物群多樣性和組成方面存在顯著差異。 值得注意的是,模型組富含 Akkermansia 和 Clostridium XVIII,而 Barnesiella 和 Alloprevotella 在 NR 組中占主導地位。 腦炎性細胞因子與模型組富集細菌呈正相關,而腦 BDNF 水平與模型組缺陷細菌呈正相關,如 Barnesiella、Alloprevotella、Prevotella、Alistipes、Mucispirillum 和 Odoribacter。 此外,從酒精處理的小鼠供體到無菌受體小鼠的糞便微生物群移植 (FMT) 導致類似的抑鬱樣行為和小膠質細胞激活狀態、細胞因子和 BDNF 水平的改變。 相反,經過 NR 處理的供體的受體小鼠與其供體具有相似的保護功能。
在一項臨床試驗中,NR 略微調節了雙胞胎的腸道微生物群組成。 長期補充 NR(每天 250–1000 毫克,持續 5 個月)增加了普拉梭菌的豐度,從而促進代謝健康和抗炎反應。 炎症性腸病 (IBD) 患者與細菌多樣性降低和產丁酸鹽細菌(如 Faecalibacterium prausnitzii)減少有關,表明腸道菌群失調在 IBD 中的重要性。 需要不同共生細菌物種之間的平衡比例來維持腸道穩態和整體宿主健康。 關聯分析表明,普氏梭菌的豐度可能有助於調節 NAD+、炎症、氨基酸和脂質代謝。
NMN 還在結腸炎實驗小鼠模型中證明了對 IBD 的保護作用,逆轉了腸道生態失調。 NMN 以 1 mg/g 體重的劑量同時給藥 21 天,或在最後 14 天用葡聚醣硫酸鈉誘導結腸炎後給藥。 除了增加微生物的豐度和多樣性外,NMN 還改善了粘液分泌和緊密連接蛋白的表達,這有助於減弱腸粘膜通透性。
長期 NMN 處理(飲用水中 0.1 至 0.6 mg/mL,持續 12 週)調節腸道微生物群的多樣性和組成,對小鼠的腸道發揮保護作用。 儘管 NMN 降低了腸道物種的多樣性,但它增加了產丁酸細菌(Ruminococcae_UCG-014 和 Prevotellaceae_NK3B31_group)和其他益生菌(如 Akkermansia muciniphila)的豐度,同時減少了幾種有害細菌(Bilophila 和 Oscillibacter)的豐度. 此外,NMN 增加了膽汁酸相關代謝物和有益代謝物的水平、杯狀細胞數量、粘液厚度和緊密連接蛋白的表達,維持了腸上皮的完整性並降低了粘膜通透性 。 牛等。 (2021) 還發現 NMN 顯著降低了糞便細菌的多樣性。 在飲用水中補充 NMN (500 mg/L (w/v)) 40 天增加了小鼠中幽門螺桿菌、粘螺旋菌和糞桿菌的豐度,並降低了變形桿菌和阿克曼氏菌的豐度。這種改變的細菌與血清成分相關 代謝產物構成,主要參與嘌呤、菸酸/煙酰胺和精氨酸/脯氨酸代謝途徑。
儘管 NAD+ 前體對腸道菌群具有潛在的調節作用,但仍需要進一步的研究來闡明它們在腸道微生物中的作用、潛在的宿主生理效應和相關機制。 最後,提高宿主 NAD+⟩ 水平是否可以促進有益腸道細菌並抑制有害細菌也有待進一步探索。
結論和未來展望
一些腸道微生物可以產生對多種疾病具有保護作用的代謝物。 來自腸道微生物群的 NMN 通過增加 NAD+ 水平和激活 AP 小鼠模型中的 SIRT3-PRDX5 通路來改善急性胰腺炎 (AP) 損傷。 腸道菌群失調會加劇 AP,其特徵是有益微生物和致病微生物之間的失衡會增加腸道通透性、細菌易位和全身炎症反應。 除了恢復腸道菌群失調外,常生糞便菌群移植 (FMT) 還誘導了血清中更高水平的 NMN,從而增強了胰腺中 NAD+ 的生物合成。 與 FMT 類似,用 NMN 預處理(500 mg/kg 體重/天腹膜內給藥,連續 28 天)增加胰腺 NAD+ 水平,以部分 SIRT3 依賴的方式減輕 AP 介導的線粒體功能障礙、氧化損傷和炎症。 這些發現表明,NMN 是 FMT 在 AP 中的保護作用的重要介質,並強化了腸道微生物群對宿主 NAD+代謝和病理障礙結果的潛在作用。
除了腸道微生物群對 B 族維生素和 NAD+ 生物合成 的活性外,最近的證據表明 NAD+ 及其前體 NR 和 NMN 對腸道微生物群的調節作用,這可能是 觀察到的有益效果。 NAD+ 前體可以通過為有益細菌提供能量來源、激活sirtuins和改善腸道屏障功能來調節腸道微生物群。
NMN 和 NR 可以選擇性地刺激雙歧桿菌和乳酸桿菌等有益菌的生長 。 這些細菌與改善腸道健康有關,包括預防腹瀉、改善腸道屏障功能、減少炎症和支持免疫系統。 此外,NAD+ 前體對去乙酰化酶的激活也可能有助於對腸道微生物群和腸道健康產生有益影響。 Sirtuins 參與調節腸道微生物群和保護腸道內皮細胞免受氧化損傷 [130]。 最後,NMN 和 NR 還可以改善腸道屏障功能,這對於防止有害細菌和毒素從腸道轉移到血液中很重要。
除了改變組成和功能特徵外,NR 對腸道微生物群的調節被證明可以防止小鼠因高脂飲食 (HFD) 引起的體重增加 。 與補充有載體(水)的對照組相比,餵食 60% HFD 並補充 0.4% NR(168 天)的小鼠體重增加減少了近 16%,空腹血糖水平也降低了近 16%。 有趣的是,從 NR 處理的供體到餵食 HFD 的小鼠的糞便移植 (FMT) 也通過降低能量效率來減輕體重增加。 膳食 NR 補充劑和 FMT-NR 補充劑均導致腸道微生物組成發生改變,具有富含產丁酸鹽的厚壁菌門的獨特功能代謝特徵。 儘管一些厚壁菌門物種與肥胖有關,但厚壁菌門的許多物種具有益生菌和抗肥胖作用 。 例如,普氏梭菌、直腸真桿菌和羅氏桿菌產生短鏈脂肪酸,包括丁酸鹽,丁酸鹽已被證明可通過抑制腸道膽固醇生物合成和促進有益的代謝作用(例如胰島素分泌、胰島素敏感性和能量消耗)來減少肥胖 。 丁酸鹽還可以通過上調肽 YY 和胰高血糖素樣肽-1 (GLP-1) 的表達來增加飽腹感和腸道流動性。 此外,FMT-NR 小鼠的盲腸內容物中 NADH 水平顯著增加,表明盲腸中的微生物代謝發生了改變。
而確實NAD+可以直接影響腸道微生物的代謝。 由於 NAD+ 是所有生物體能量代謝的重要組成部分,主要是許多參與細胞 ATP 產生的關鍵酶的輔助因子,因此增加 NAD+ 可能會促進微生物的能量生產。 此外,NAD+可以通過關鍵的抑制性神經遞質 β-NAD 調節結腸的運動,並通過影響宿主膽汁酸的合成來間接影響腸道微生物,當它們破壞細菌細胞膜時可以發揮抗菌作用給小鼠膳食補充 NR 10 週(每天 400 mg/kg)可降低促炎和抗炎細胞因子水平,抑制小膠質細胞活化,並防止酒精引起的抑鬱樣行為。 這種效應歸因於 NR 通過改變腸道微生物群組成來上調腦源性神經營養因子 (BDNF) 的能力。 與對照組和 NR 組相比,酒精引起的抑鬱症小鼠模型在腸道微生物群多樣性和組成方面存在顯著差異。 值得注意的是,模型組富含 Akkermansia 和 Clostridium XVIII,而 Barnesiella 和 Alloprevotella 在 NR 組中占主導地位。 腦炎性細胞因子與模型組富集細菌呈正相關,而腦 BDNF 水平與模型組缺陷細菌呈正相關,如 Barnesiella、Alloprevotella、Prevotella、Alistipes、Mucispirillum 和 Odoribacter。 此外,從酒精處理的小鼠供體到無菌受體小鼠的糞便微生物群移植 (FMT) 導致類似的抑鬱樣行為和小膠質細胞激活狀態、細胞因子和 BDNF 水平的改變。 相反,經過 NR 處理的供體的受體小鼠與其供體具有相似的保護功能。
在一項臨床試驗中,NR 略微調節了雙胞胎的腸道微生物群組成。 長期補充 NR(每天 250–1000 毫克,持續 5 個月)增加了普拉梭菌的豐度,從而促進代謝健康和抗炎反應。 炎症性腸病 (IBD) 患者與細菌多樣性降低和產丁酸鹽細菌(如 Faecalibacterium prausnitzii)減少有關,表明腸道菌群失調在 IBD 中的重要性。 需要不同共生細菌物種之間的平衡比例來維持腸道穩態和整體宿主健康。 關聯分析表明,普氏梭菌的豐度可能有助於調節 NAD+、炎症、氨基酸和脂質代謝。
NMN 還在結腸炎實驗小鼠模型中證明了對 IBD 的保護作用,逆轉了腸道生態失調。 NMN 以 1 mg/g 體重的劑量同時給藥 21 天,或在最後 14 天用葡聚醣硫酸鈉誘導結腸炎後給藥。 除了增加微生物的豐度和多樣性外,NMN 還改善了粘液分泌和緊密連接蛋白的表達,這有助於減弱腸粘膜通透性。
長期 NMN 處理(飲用水中 0.1 至 0.6 mg/mL,持續 12 週)調節腸道微生物群的多樣性和組成,對小鼠的腸道發揮保護作用。 儘管 NMN 降低了腸道物種的多樣性,但它增加了產丁酸細菌(Ruminococcae_UCG-014 和 Prevotellaceae_NK3B31_group)和其他益生菌(如 Akkermansia muciniphila)的豐度,同時減少了幾種有害細菌(Bilophila 和 Oscillibacter)的豐度. 此外,NMN 增加了膽汁酸相關代謝物和有益代謝物的水平、杯狀細胞數量、粘液厚度和緊密連接蛋白的表達,維持了腸上皮的完整性並降低了粘膜通透性 。 牛等。 (2021) 還發現 NMN 顯著降低了糞便細菌的多樣性。 在飲用水中補充 NMN (500 mg/L (w/v)) 40 天增加了小鼠中幽門螺桿菌、粘螺旋菌和糞桿菌的豐度,並降低了變形桿菌和阿克曼氏菌的豐度。這種改變的細菌與血清成分相關 代謝產物構成,主要參與嘌呤、菸酸/煙酰胺和精氨酸/脯氨酸代謝途徑。
儘管 NAD+ 前體對腸道菌群具有潛在的調節作用,但仍需要進一步的研究來闡明它們在腸道微生物中的作用、潛在的宿主生理效應和相關機制。 最後,提高宿主 NAD+⟩ 水平是否可以促進有益腸道細菌並抑制有害細菌也有待進一步探索。
結論和未來展望
NR 和 NMN 在食品中的天然存在,以及它們對動物和人類的潛在有益影響,正在食品科學和營養領域開闢一個令人興奮的新領域。 調查它們在膳食來源中的含量以及生物可及性肯定證明了研究工作的合理性。
尋找 NMN 和 NR 的潛在食物來源,從常見的消費品到廢棄的副產品,可以為改善飲食和開發功能性食品提供見解。 此外,這可能會導致識別用於這些化合物的提取、分離和生物技術生產的新原材料。 評估可以保持和增強 NR 和 NMN 的生理益處的食品加工策略也很重要。
NAD+前體在各種組織和細胞內的代謝和生物分佈仍然知之甚少。 需要進一步的研究來調查膳食 NMN 和 NR 的生物利用度、定量代謝組學和藥代動力學。 這些研究可以幫助確定每種前體在維持和提高 NAD+ 水平方面的最佳劑量和貢獻,以及它們通過飲食產生的生理效應。
最後,鑑於腸道微生物群在人類健康中的關鍵作用以及 NMN 和 NR 調節腸道微生物的新證據,有必要研究腸道微生物群代謝與 NR 和 NMN 之間的串擾。 這些研究可以幫助確定對健康的潛在影響,並提供對潛在機制的見解。
尋找 NMN 和 NR 的潛在食物來源,從常見的消費品到廢棄的副產品,可以為改善飲食和開發功能性食品提供見解。 此外,這可能會導致識別用於這些化合物的提取、分離和生物技術生產的新原材料。 評估可以保持和增強 NR 和 NMN 的生理益處的食品加工策略也很重要。
NAD+前體在各種組織和細胞內的代謝和生物分佈仍然知之甚少。 需要進一步的研究來調查膳食 NMN 和 NR 的生物利用度、定量代謝組學和藥代動力學。 這些研究可以幫助確定每種前體在維持和提高 NAD+ 水平方面的最佳劑量和貢獻,以及它們通過飲食產生的生理效應。
最後,鑑於腸道微生物群在人類健康中的關鍵作用以及 NMN 和 NR 調節腸道微生物的新證據,有必要研究腸道微生物群代謝與 NR 和 NMN 之間的串擾。 這些研究可以幫助確定對健康的潛在影響,並提供對潛在機制的見解。
Curr Nutr Rep. 2023 Jun 5 : 1–20.
doi: 10.1007/s13668-023-00475-y [Epub ahead of print]
PMCID: PMC10240123
PMID: 37273100
NAD+ Precursors Nicotinamide Mononucleotide (NMN) and Nicotinamide Riboside (NR): Potential Dietary Contribution to Health
Gabriela Fabiana Soares Alegre and Glaucia Maria Pastore
doi: 10.1007/s13668-023-00475-y [Epub ahead of print]
PMCID: PMC10240123
PMID: 37273100
NAD+ Precursors Nicotinamide Mononucleotide (NMN) and Nicotinamide Riboside (NR): Potential Dietary Contribution to Health
Gabriela Fabiana Soares Alegre and Glaucia Maria Pastore