NMN 生成酶驅動與斷食相關的脂肪燃燒 (2022/02)
聖路易斯華盛頓大學醫學院的研究人員表明,NMN 生物合成背後的酶 NAMPT可逆轉肥胖小鼠的代謝紊亂。
要點
1.NAMPT (煙醯胺磷酸核糖基催化酶)是一種產生 NMN 的酶,它需要增強代謝應激小鼠的脂肪(脂質)和糖(葡萄糖)的平衡。
2.在糖尿病小鼠中,NAMPT 會增加產熱——生物體燃燒卡路里以產生熱量的代謝過程。
3.這些數據強調了 NAMPT 激活和 NMN 在肝細胞中的直接治療作用,以模擬斷食的效果。
間歇性禁食和熱量限制可改善小鼠和人類的新陳代謝和炎症。 這就是為什麼間歇性禁食和熱量限制都被視為減輕衰老、營養過剩和神經退行性疾病的有希望的方法的原因。 熱量限制通過激活代謝信號通路(包括煙酰胺腺嘌呤二核苷酸 (NAD+) 合成通路)來減輕衰老和心臟代謝疾病。
聖路易斯華盛頓大學醫學院的研究人員發表在《自然通訊》(Nature Communications)上,表明 NAMPT——一種合成 NAD+ 前體 NMN 所必需的酶——在肝臟中驅動了禁食反應的關鍵方面。 一方面,肝細胞中缺乏 NAMPT 的小鼠在禁食期間表現出熱調節缺陷,並對飲食誘導的葡萄糖不耐受敏感。 另一方面,肝細胞中 NAMPT 水平的增加會誘導肥胖小鼠的脂肪褐變、改善葡萄糖平衡並減輕高血脂水平(血脂異常)。 這項工作表明,調節肝細胞中的 NAD+ 水平可以潛在地減輕與斷食相關的疾病。
1.NAMPT (煙醯胺磷酸核糖基催化酶)是一種產生 NMN 的酶,它需要增強代謝應激小鼠的脂肪(脂質)和糖(葡萄糖)的平衡。
2.在糖尿病小鼠中,NAMPT 會增加產熱——生物體燃燒卡路里以產生熱量的代謝過程。
3.這些數據強調了 NAMPT 激活和 NMN 在肝細胞中的直接治療作用,以模擬斷食的效果。
間歇性禁食和熱量限制可改善小鼠和人類的新陳代謝和炎症。 這就是為什麼間歇性禁食和熱量限制都被視為減輕衰老、營養過剩和神經退行性疾病的有希望的方法的原因。 熱量限制通過激活代謝信號通路(包括煙酰胺腺嘌呤二核苷酸 (NAD+) 合成通路)來減輕衰老和心臟代謝疾病。
聖路易斯華盛頓大學醫學院的研究人員發表在《自然通訊》(Nature Communications)上,表明 NAMPT——一種合成 NAD+ 前體 NMN 所必需的酶——在肝臟中驅動了禁食反應的關鍵方面。 一方面,肝細胞中缺乏 NAMPT 的小鼠在禁食期間表現出熱調節缺陷,並對飲食誘導的葡萄糖不耐受敏感。 另一方面,肝細胞中 NAMPT 水平的增加會誘導肥胖小鼠的脂肪褐變、改善葡萄糖平衡並減輕高血脂水平(血脂異常)。 這項工作表明,調節肝細胞中的 NAD+ 水平可以潛在地減輕與斷食相關的疾病。
肝臟是代謝調節的核心
肝臟獨特地位於來自消化系統的血液和被送回心臟以泵送到大腦、四肢和身體其他部位的血液之間的連接處。 在這裡,肝臟可以感知、協調和轉換依賴於進食或缺乏(也稱為斷食)的不同代謝狀態。 養分撤退對一個有機體,特別是對肝細胞來說,是一個適應或滅亡的命題。 糖的缺乏迫使依賴於全身的脂肪分解,脂肪在肝臟中代謝。 當這種情況發生時,肝臟需要做出幾個關鍵的調整。 NAD+ 合成統一了對營養受限肝臟中每種壓力的適應性反應。 因此,NAD+ 可以預防各種疾病,從衰老和神經退行性變到糖尿病和非酒精性脂肪肝 (NAFLD)。
肝臟 NAMPT 是斷食益處所必需的
在這項研究中,聖路易斯華盛頓醫科大學的研究人員剖析了肝細胞中的 NAMPT 如何調節代謝平衡。 Higgins 及其同事證明,肝臟 NAMPT 在斷食期間介導了一個關鍵的肝臟信號級聯反應。 該研究表明,斷食和葡萄糖轉運抑制會上調肝臟中的 NAMPT,而肝臟特異性 NAMPT 缺乏會損害幾個關鍵的空腹代謝過程。 更具體地說,肝臟中缺乏 NAMPT 的小鼠表現出葡萄糖代謝缺陷,而病毒介導的肝臟 NAMPT 增加增強了飲食誘導和遺傳肥胖模型中的產熱和葡萄糖代謝。 這些發現表明,肝臟 NAMPT 水平對於防止飲食引起的葡萄糖耐受不良和引發斷食的代謝益處至關重要。
肝臟獨特地位於來自消化系統的血液和被送回心臟以泵送到大腦、四肢和身體其他部位的血液之間的連接處。 在這裡,肝臟可以感知、協調和轉換依賴於進食或缺乏(也稱為斷食)的不同代謝狀態。 養分撤退對一個有機體,特別是對肝細胞來說,是一個適應或滅亡的命題。 糖的缺乏迫使依賴於全身的脂肪分解,脂肪在肝臟中代謝。 當這種情況發生時,肝臟需要做出幾個關鍵的調整。 NAD+ 合成統一了對營養受限肝臟中每種壓力的適應性反應。 因此,NAD+ 可以預防各種疾病,從衰老和神經退行性變到糖尿病和非酒精性脂肪肝 (NAFLD)。
肝臟 NAMPT 是斷食益處所必需的
在這項研究中,聖路易斯華盛頓醫科大學的研究人員剖析了肝細胞中的 NAMPT 如何調節代謝平衡。 Higgins 及其同事證明,肝臟 NAMPT 在斷食期間介導了一個關鍵的肝臟信號級聯反應。 該研究表明,斷食和葡萄糖轉運抑制會上調肝臟中的 NAMPT,而肝臟特異性 NAMPT 缺乏會損害幾個關鍵的空腹代謝過程。 更具體地說,肝臟中缺乏 NAMPT 的小鼠表現出葡萄糖代謝缺陷,而病毒介導的肝臟 NAMPT 增加增強了飲食誘導和遺傳肥胖模型中的產熱和葡萄糖代謝。 這些發現表明,肝臟 NAMPT 水平對於防止飲食引起的葡萄糖耐受不良和引發斷食的代謝益處至關重要。
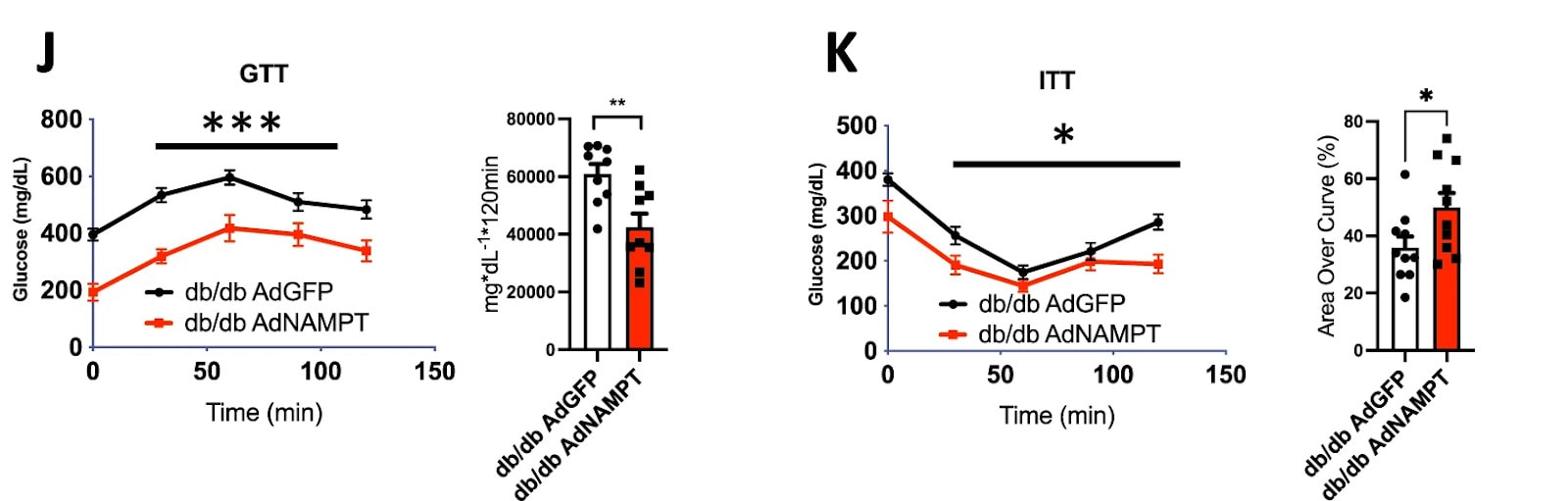
(Higgins et al., 2022 | Nature Communications) 肝臟 NAMPT 可增強糖尿病小鼠的葡萄糖穩態。 肥胖、糖尿病小鼠 (db/db AdNAMPT) 中 NAMPT 水平的增加導致整個葡萄糖和胰島素耐量測試中的血漿葡萄糖降低,表明葡萄糖代謝和胰島素敏感性得到改善。
Higgins 及其同事發現,提高肥胖糖尿病小鼠的 NAMPT 水平會增加脂肪組織褐變標誌物。 脂肪組織(通常是白色)在生熱活躍時會變成棕色,這意味著它在燃燒卡路里的同時會產生更多的熱量。 沿著這些思路,肝臟 NAMPT 升高的小鼠的產熱水平高於對照組。 提高肝細胞 NAMPT 會導緻小鼠在光循環和暗循環期間增加熱量產生和氣體交換——在呼吸過程中更多的氧氣和二氧化碳排出——而 NAMPT 缺失會導致暗循環熱缺陷。 數據表明,肝細胞 NAMPT 信號在調節能量控制時可區分光週期和暗週期。
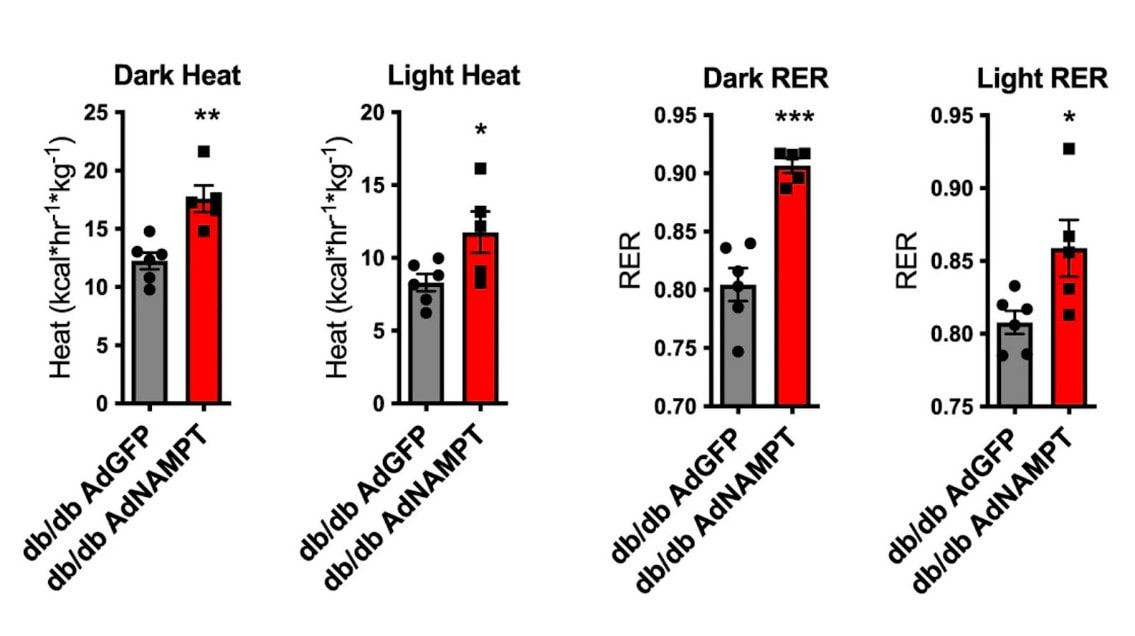
(Higgins et al., 2022 | Nature Communications) NAMPT 在糖尿病小鼠中誘導脂肪組織褐變和產熱。 為了測量 NAMPT 在產熱和能量調節中的作用,糖尿病小鼠 (db/db) 接受了攜帶 NAMPT 的病毒 (AdNAMPT) 的治療。 與對照組相比,這些小鼠表現出明顯更高的暗循環和光循環產熱和呼吸交換率 (RER)。
Higgins 及其同事得出結論,肝臟中的 NAMPT 在肝細胞中廣泛斷食和葡萄糖轉運抑制的下游發揮廣泛的斷食模擬效應。 這項研究表明,代謝疾病可以通過 NMN 在 NAD+ 生物合成水平上進行干預。 肝臟中的 NAMPT 激活可能可以對抗衰老、肥胖和其他空腹反應性疾病。 有趣的是,有一些化合物可以激活 NAMPT,例如 SBI-797812,它將 NAMPT 變成更有效地生成 NMN 的“超級催化劑”。 值得注意的是,服用 SBI-797812 的小鼠肝臟 NAD+ 升高。 據我們所知,這可能是長期以來備受追捧的奇蹟禁食丸的基礎。