犬尿氨酸途徑(KP)和 NAD+ 代謝在
肌痛性腦脊髓炎/慢性疲勞綜合症(ME/CFS)中的作用 (2022/01)
摘要
肌痛性腦脊髓炎/慢性疲勞綜合徵 (ME/CFS) 是一種嚴重、複雜和高度衰弱的長期疾病。患有 ME/CFS 的人通常無法進行日常活動。該疾病的主要標誌是神經和胃腸道功能障礙,伴有普遍的不適,在身體和/或精神活動後會加劇。目前,還沒有針對這種疾病的生物標誌物簽名的有效治愈方法。受損的色氨酸 (TRYP) 代謝被認為在 ME/CFS 的病理生物學中起重要作用。 TRYP 是血清素和必需的煙酰胺腺嘌呤二核苷酸 (NAD+) 的重要前體。 TRYP 與負責行為功能的大腦某些部分的發育有關。 TRYP 的主要分解代謝途徑是犬尿氨酸途徑 (KP)。 KP 產生 NAD+ 和幾種具有神經保護(即犬尿酸(KYNA))和神經毒性(即喹啉酸(QUIN))活性的神經活性代謝物。 KP 的過度激活,無論是代償性還是退化的驅動機制,都可以限制 NAD+ 的可用性並加劇 ME/CFS 的症狀。本綜述討論了 ME/CFS 中 KP 代謝改變的潛在關聯。該評價還評估了患者腸道微生物群對 TRYP 可用性和 KP 激活的作用。我們提出旨在提高 NAD+ 水平的策略(例如,使用煙酰胺單核苷酸和煙酰胺核苷)可能是克服疲勞症狀和改善 ME/CFS 患者生活質量的有希望的干預措施。未來的臨床試驗應進一步評估 NAD+ 補充劑在減少 ME/CFS 的某些臨床特徵方面的潛在益處。
肌痛性腦脊髓炎/慢性疲勞綜合徵 (ME/CFS) 是一種嚴重、複雜和高度衰弱的長期疾病。患有 ME/CFS 的人通常無法進行日常活動。該疾病的主要標誌是神經和胃腸道功能障礙,伴有普遍的不適,在身體和/或精神活動後會加劇。目前,還沒有針對這種疾病的生物標誌物簽名的有效治愈方法。受損的色氨酸 (TRYP) 代謝被認為在 ME/CFS 的病理生物學中起重要作用。 TRYP 是血清素和必需的煙酰胺腺嘌呤二核苷酸 (NAD+) 的重要前體。 TRYP 與負責行為功能的大腦某些部分的發育有關。 TRYP 的主要分解代謝途徑是犬尿氨酸途徑 (KP)。 KP 產生 NAD+ 和幾種具有神經保護(即犬尿酸(KYNA))和神經毒性(即喹啉酸(QUIN))活性的神經活性代謝物。 KP 的過度激活,無論是代償性還是退化的驅動機制,都可以限制 NAD+ 的可用性並加劇 ME/CFS 的症狀。本綜述討論了 ME/CFS 中 KP 代謝改變的潛在關聯。該評價還評估了患者腸道微生物群對 TRYP 可用性和 KP 激活的作用。我們提出旨在提高 NAD+ 水平的策略(例如,使用煙酰胺單核苷酸和煙酰胺核苷)可能是克服疲勞症狀和改善 ME/CFS 患者生活質量的有希望的干預措施。未來的臨床試驗應進一步評估 NAD+ 補充劑在減少 ME/CFS 的某些臨床特徵方面的潛在益處。
1.簡介
肌痛性腦脊髓炎/慢性疲勞綜合徵 (ME/CFS) 是一種複雜的多系統、長期、致殘性疾病。 ME/CFS 的主要標誌是使人衰弱的疲勞,這種疲勞至少存在 6 個月,並且不會因休息而得到改善。 根據醫學研究所 (IOM) 的報告,美國有 83,000 至 250 萬人患有 ME/CFS,估計每年的經濟負擔為 17-240 億美元。據估計,ME/CFS 的患病率為澳大利亞人的 0.4-1%,這意味著多達 250,000 人受到影響。這種疾病的特點是與認知、免疫系統、自主功能和內分泌系統受損相關的複雜症狀(圖 1)。患有 ME/CFS 的人會遭受極度疲勞、頭暈和睡眠障礙。這種疾病會影響所有種族和年齡,女性的風險是男性的三到四倍。由於臨床上沒有特定的實驗室診斷標誌物或明確的測試,許多患者沒有得到迅速診斷。通過在分子和臨床水平上解開 ME/CFS 的病理生物學,已經做出了努力來解決這個問題。
圖一 ME/CFS 患者的常見症狀和顯著特徵。
ME / CFS的病因也知之甚少。主要問題是 ME/CFS 通常在個體已經處於嚴重階段時被診斷出來。大約 50-80% 的患者表現出突然的、持續的流感樣症狀。 ME/CFS 通常發生在細菌或病毒感染後。這些感染可能使免疫系統功能失調,引發 ME/CFS,隨後出現可能長期持續的多系統損傷。正如 SARS 流行後觀察到的那樣,我們推測更多的 COVID-19 患者可能會增加報告的 ME/CFS 病例 。
關於 ME/CFS 的病理生理學,許多研究報告了 5-羥色胺能係統功能障礙、慢性病毒感染以及免疫反應(即免疫激活和慢性炎症)和細胞生物能學異常的證據。下丘腦室旁核附近的慢性神經炎症是 ME/CFS 的一個重要因素。來自先進分子技術的證據表明,細胞因子產生、免疫激活和炎症的增加與細胞能量代謝和線粒體功能的缺陷有關。免疫激活可以通過犬尿氨酸途徑 (KP) 增加色氨酸 (TRYP) 代謝的通量,通過實現誘導吲哚胺 2,3-雙加氧酶 1 (IDO-1)(KP 中的主要酶)活性的促炎細胞因子。高達 90% 的 TRYP 通過 KP 分解代謝成神經活性代謝物和煙酰胺腺嘌呤二核苷酸 (NAD+)。來自 KP 的 TRYP 分解代謝的代謝物與炎症、免疫反應和神經系統疾病有關。值得一提的是,KP 活性的任何增加都會使 TRYP 從血清素途徑中分流。 5-羥色胺通路的下調可能導致 ME/CFS 症狀的出現,例如慢性疲勞、抑鬱、睡眠問題和頭痛。
本研究是一項全面審查,i) 討論了 KP 與 ME/CFS 的可能關聯; ii) 強調患者腸道菌群在 TRYP 可用性中的作用; iii) 強調 KP 代謝物的重要性及其與疾病症狀的關係,以及 iv) 評估提高 NAD+ 前體水平以減輕疾病症狀的作用的證據。 通過傳播這些信息,本綜述旨在為該領域的研究人員提供一個有前途的治療概念,並使我們更接近開發 ME/CFS 的生物印記。
關於 ME/CFS 的病理生理學,許多研究報告了 5-羥色胺能係統功能障礙、慢性病毒感染以及免疫反應(即免疫激活和慢性炎症)和細胞生物能學異常的證據。下丘腦室旁核附近的慢性神經炎症是 ME/CFS 的一個重要因素。來自先進分子技術的證據表明,細胞因子產生、免疫激活和炎症的增加與細胞能量代謝和線粒體功能的缺陷有關。免疫激活可以通過犬尿氨酸途徑 (KP) 增加色氨酸 (TRYP) 代謝的通量,通過實現誘導吲哚胺 2,3-雙加氧酶 1 (IDO-1)(KP 中的主要酶)活性的促炎細胞因子。高達 90% 的 TRYP 通過 KP 分解代謝成神經活性代謝物和煙酰胺腺嘌呤二核苷酸 (NAD+)。來自 KP 的 TRYP 分解代謝的代謝物與炎症、免疫反應和神經系統疾病有關。值得一提的是,KP 活性的任何增加都會使 TRYP 從血清素途徑中分流。 5-羥色胺通路的下調可能導致 ME/CFS 症狀的出現,例如慢性疲勞、抑鬱、睡眠問題和頭痛。
本研究是一項全面審查,i) 討論了 KP 與 ME/CFS 的可能關聯; ii) 強調患者腸道菌群在 TRYP 可用性中的作用; iii) 強調 KP 代謝物的重要性及其與疾病症狀的關係,以及 iv) 評估提高 NAD+ 前體水平以減輕疾病症狀的作用的證據。 通過傳播這些信息,本綜述旨在為該領域的研究人員提供一個有前途的治療概念,並使我們更接近開發 ME/CFS 的生物印記。
2. ME/CFS的流行病學
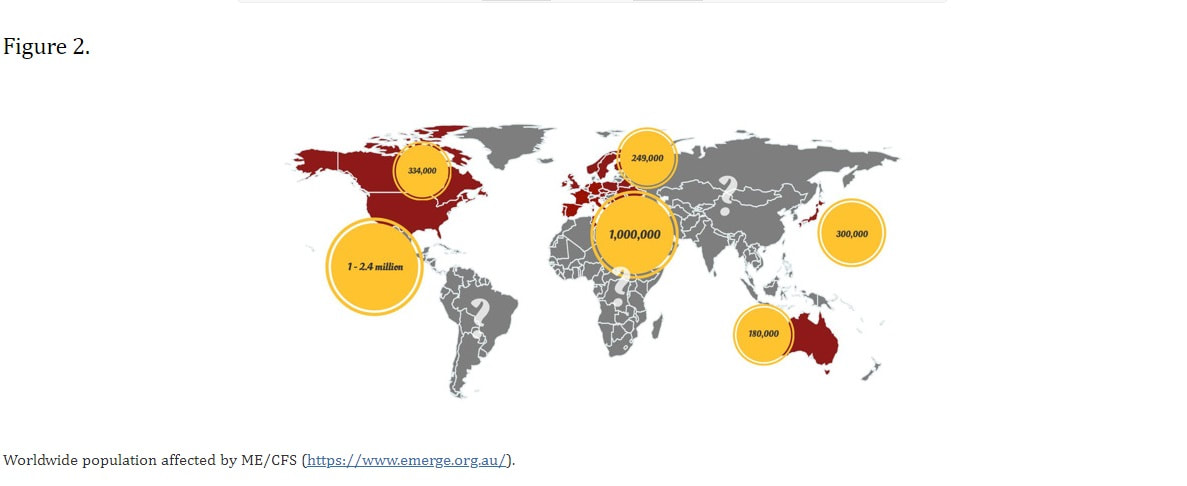
ME/CFS 的確切患病率仍然存在爭議;然而,大量研究報告了成人 ME/CFS 的顯著患病率。這一爭議是由於多種因素造成的,包括實驗室方法的差異以及為定義和確定疾病而調查的人群類型。因此,ME/CFS 研究中的通用診斷標準是必不可少的,但缺乏。應注意將患有已知病理疾病的個體排除為 ME/CFS 患者。 根據加拿大隱私專員辦公室 (OPC) 的數據,英國約 27% 的成年人患有慢性疲勞,佔該人群的 13.4%。在英格蘭進行的一項研究顯示,在 143,000 名個體(年齡 18-64 歲)中,CFS 的發病率為 4.7%(流行率為 0.2%)。美國的另一項研究估計,超過 6% 的人會經歷持續 14 天以上的嚴重疲勞。根據當前疾病控制和預防中心 (CDC) 的統計數據,美國有超過 100 萬人患有 ME/CFS。根據堪薩斯州威奇託的一項為期四年的研究,CFS 的患病率為每 100,000 人 235 人,女性的患病率是男性的四倍。勞裡等人。 (1997) 報告說,愛丁堡疲勞綜合徵的年發病率和患病率分別為每 100,000 人 370 人和每 100,000 人 740 人。雖然該疾病的定義和分類各不相同,並且會影響患病率報告,但據估計,大約 0.4-1% 的澳大利亞人患有 ME/CFS。挪威的一項研究確定了 ME/CFS 年齡患病率的兩個高峰。第一個出現在 10 到 19 歲之間,另一個出現在 30 到 39 歲之間。總體而言,據估計,全世界約有 17-2400 萬人患有 ME/CFS(圖 2),其中女性的風險高出四倍。
圖二 受 ME/CFS 影響的全球人口 (https://www.emerge.org.au/)。
大約四分之一的患者完全殘疾,估計每人每年花費 20,000 美元。 由於症狀複雜,患者的癒後具有挑戰性。 在大多數情況下,症狀的改善比完全康復更常見。 患有嚴重 ME/CFS 的患者通常死於潛在的健康並發症,例如心血管疾病和癌症。
3.ME/CFS的病因和病理生理學
多項臨床研究表明,感染、遺傳、身體創傷、壓力和環境是發生 ME/CFS 的危險因素。 ME/CFS 患者有幾種影響各種器官系統的病理生理異常。然而,尚不清楚這些異常是發生在 ME/CFS 之後還是疾病的始作俑者。 ME / CFS中可能的免疫系統異常可能包括促炎細胞因子(即IL-4,IL-5,IL-6,IL-12)的產生增加,由於功能失調的自然殺傷細胞(NK)引起的免疫抑制,減少T 細胞的功能(例如 CD8+ 和 CD4+),並增加自身抗體(例如風濕因子、抗甲狀腺)的產生。 ME/CFS 的嚴重程度可能與功能不佳的 NK 細胞有關。 NK細胞在病毒劫持細胞的初級識別和破壞中起關鍵作用。據報導,在幾個案例中,由於 NK 細胞功能低下,ME/CFS 對由 Epstein-Barr 病毒、鉅細胞病毒和人類皰疹病毒 1、6 和 7 型引起的病毒感染的易感性可能會增加。反過來,這些感染可能會引起炎症和/或大大限制 NAD+ 的產生。例如,人類皰疹病毒 1 型感染可引發聚 (ADP-核糖) 糖水解酶的降解和 NAD 依賴性 DNA 切口傳感器聚 (ADP-核糖) 聚合酶 (PARP) 的激活。後一種酶在修復雙鏈 DNA 的損傷時會消耗 NAD+ 。
ME/CFS 患者的慢性炎症和氧化應激也可能是由促炎細胞因子的產生增加、抗氧化化合物(例如輔酶 Q10)和抗氧化酶水平降低、氧化和亞硝化水平增加引起的應激(IO&NS),對重要大分子(例如 DNA、蛋白質、脂肪酸)的損傷、線粒體功能障礙和細胞凋亡途徑的過度激活。 ME / CFS期間促炎細胞因子水平的增加可以解釋觀察到的疲勞和流感樣症狀。然而,最普遍接受的 ME/CFS 炎症假設是傳染性的,特別是病毒起源,作為誘導抗病毒免疫反應和全身炎症的補償機制。
高達 60% 的 ME/CFS 患者俱有高滴度的自身抗體 。結果表明,ME/CFS 患者對由氧化和亞硝化應激誘導的過氧化作用和 S-法呢基-l-半胱氨酸產生的一些通常不具有免疫原性的降解膜脂產生 IgM 相關免疫反應。有人提出,可能由感染引起的慢性免疫系統激活和炎症可能導致 ME/CFS 患者的這些自身免疫並發症 [46, 59]。促炎細胞因子的產生增加,例如 IL-1 和腫瘤壞死因子-α (TNFα),以及核因子-κB 水平的升高進一步惡化了自身免疫狀況。效應 B 細胞和自身反應性 T 細胞的數量隨著異常細胞因子的產生而增加。相反,NK細胞數量減少,引發體內平衡失衡並提高效應T細胞的存活率。通常在 ME/CFS 患者中觀察到的病毒感染可以通過使用分子模擬來引發自身免疫。此外,在這些患者中也可見到的細菌易位可誘發自身免疫和炎症。自身免疫也可由線粒體功能障礙和乾擾細胞凋亡和壞死的 NAD+ 和 ATP 水平降低介導。還發現 ME/CFS 患者俱有針對神經遞質和中樞神經系統 (CNS) 中重要成分的自身抗體,包括血清素、多巴胺、神經節苷脂、毒蕈鹼受體和 5-羥色胺受體 1A 受體。這些異常可以解釋神經系統相關症狀的存在,例如慢性疲勞、認知障礙和睡眠障礙。
ME/CFS 患者的慢性炎症和氧化應激也可能是由促炎細胞因子的產生增加、抗氧化化合物(例如輔酶 Q10)和抗氧化酶水平降低、氧化和亞硝化水平增加引起的應激(IO&NS),對重要大分子(例如 DNA、蛋白質、脂肪酸)的損傷、線粒體功能障礙和細胞凋亡途徑的過度激活。 ME / CFS期間促炎細胞因子水平的增加可以解釋觀察到的疲勞和流感樣症狀。然而,最普遍接受的 ME/CFS 炎症假設是傳染性的,特別是病毒起源,作為誘導抗病毒免疫反應和全身炎症的補償機制。
高達 60% 的 ME/CFS 患者俱有高滴度的自身抗體 。結果表明,ME/CFS 患者對由氧化和亞硝化應激誘導的過氧化作用和 S-法呢基-l-半胱氨酸產生的一些通常不具有免疫原性的降解膜脂產生 IgM 相關免疫反應。有人提出,可能由感染引起的慢性免疫系統激活和炎症可能導致 ME/CFS 患者的這些自身免疫並發症 [46, 59]。促炎細胞因子的產生增加,例如 IL-1 和腫瘤壞死因子-α (TNFα),以及核因子-κB 水平的升高進一步惡化了自身免疫狀況。效應 B 細胞和自身反應性 T 細胞的數量隨著異常細胞因子的產生而增加。相反,NK細胞數量減少,引發體內平衡失衡並提高效應T細胞的存活率。通常在 ME/CFS 患者中觀察到的病毒感染可以通過使用分子模擬來引發自身免疫。此外,在這些患者中也可見到的細菌易位可誘發自身免疫和炎症。自身免疫也可由線粒體功能障礙和乾擾細胞凋亡和壞死的 NAD+ 和 ATP 水平降低介導。還發現 ME/CFS 患者俱有針對神經遞質和中樞神經系統 (CNS) 中重要成分的自身抗體,包括血清素、多巴胺、神經節苷脂、毒蕈鹼受體和 5-羥色胺受體 1A 受體。這些異常可以解釋神經系統相關症狀的存在,例如慢性疲勞、認知障礙和睡眠障礙。
4.色氨酸代謝(TRYP)和犬尿氨酸途徑(KP)
TRYP 是一種必需氨基酸,是各種生物活性分子的前體,其中最值得注意的是血清素。然而,一小部分 TRYP 被轉化為血清素,其中超過 90% 被代謝為犬尿氨酸 (KYN)、幾種下游神經活性代謝物和 NAD+ 的從頭合成。 KP 由促炎細胞因子如 INFγ 強烈誘導。包括色氨酸雙加氧酶 (TDO) 和 IDO-1 在內的兩種重要酶催化 KP 的第一個限速步驟,即 TRYP 轉化為 KYN。 TDO 主要在肝臟中表達,而 IDO-1 存在於許多細胞中,例如巨噬細胞和腦細胞。在正常生理條件下,KYN主要通過犬尿氨酸單加氧酶(KMO)的催化活性轉化為3-羥基犬尿氨酸(3-HK)。在接下來的步驟中,3-HK 被代謝為 3-羥基鄰氨基苯甲酸 (3HAA)、喹啉酸 (QUIN),最後是 NAD+。剩餘的 KYN 也通過犬尿氨酸氨基轉移酶 (KAT) 同工酶轉化為犬尿酸 (KYNA)。 KYNA 被稱為神經保護代謝物,可拮抗 QUIN 的興奮毒性潛能(圖 3)。
圖三 犬尿氨酸途徑和 NAD+ 補救途徑。
IDO:吲哚胺-吡咯2,3-雙加氧酶;
TDO:色氨酸 2,3-雙加氧酶;
KATs:犬尿氨酸氨基轉移酶;
KMO:犬尿氨酸3-單加氧酶;
3HAO:3-羥基鄰氨基苯甲酸氧化酶;
QPRT:喹啉磷酸核糖基轉移酶;
ACMSD:ACMS 脫羧酶。
IDO:吲哚胺-吡咯2,3-雙加氧酶;
TDO:色氨酸 2,3-雙加氧酶;
KATs:犬尿氨酸氨基轉移酶;
KMO:犬尿氨酸3-單加氧酶;
3HAO:3-羥基鄰氨基苯甲酸氧化酶;
QPRT:喹啉磷酸核糖基轉移酶;
ACMSD:ACMS 脫羧酶。
4.1 ME/CFS 中色氨酸代謝的改變
4.1.1 抑鬱和情緒障礙
多項研究提供的證據表明 IDO-1 的過度激活和隨後的 TRYP 消耗可能與抑鬱和其他情緒障礙有關。情緒障礙是 ME/CFS 患者常見的並發症。 IDO-1 在不同的人體組織中廣泛表達,包括腎、腦、肺、樹突狀細胞和巨噬細胞。它由 IFN-γ、TNFα、IL-1β、澱粉樣蛋白 β 和脂多醣誘導。有充分證據表明,情緒障礙與細胞介導的免疫系統激活有關,並伴有炎症增加、IFN-γ、IL-1β 和 TNFα 的產生。這些促炎細胞因子可以強烈激活KP。 KP 的過度激活將 TRYP 從 5-羥色胺生物合成途徑中轉移,從而消耗 5-羥色胺水平,同時刺激 KP 代謝物的過度生產。應該注意的是,KYN 具有抑製作用,而 KYNA 是一種神經保護代謝物。因此,KYN 與 KYNA 的比率是 KAT 活性和神經毒性潛力的重要指標。因此,Maes 等人。 (2011) 報告說,抑鬱症狀,尤其是軀體化,與 KYN:KYNA 和 KYN:TRYP 比率指定的血清 KP 代謝物水平升高直接相關,與血清中血清 TRYP 水平呈負相關.
KYN 向 KYNA 的轉化減少可能是由於神經膠質抑制因子下調 KAT-I 的活性。這種現象會導致 KYN 和 QUIN 水平過高。或者,KYN:KYNA 比率的增加可以通過炎症期間小膠質細胞對星形膠質細胞的影響來證明。在 ME/CFS 患者中廣泛觀察到的慢性炎症會激活小膠質細胞和星形膠質細胞。這些細胞被認為是 TRYP 分解代謝的主要部位 。星形膠質細胞是主要的 KYNA 生產細胞,而小膠質細胞是主要的 QUIN 生產者。小膠質細胞激活誘導大腦中的 KP 並產生促炎介質。激活的小膠質細胞過度產生 QUIN 反過來又通過抑制星形膠質細胞來降低 KYNA 水平。據報導,抑鬱症患者的小膠質細胞數量多,星形膠質細胞滴度低。有人提出小膠質細胞在 ME/CFS 患者的大部分大腦中被激活。因此,Nakatomi 等人 (2014) 報導了與 ME/CFS 患者相比,11C-(R)-PK11195(一種由活化小膠質細胞表達的轉運蛋白的配體)的結合電位值增加。健康的對照。
小膠質細胞激活還可以通過釋放 IL-1β 觸發星形膠質細胞中血清素轉運蛋白 (5-HTT) 的上調,從而降低細胞外血清素水平,從而導致抑鬱症。從小膠質細胞釋放的 IL-1β 與星形膠質細胞 5-HTT 之間的相互作用是眾所周知的,通過使用 IL-1 受體拮抗劑證明了這一點。 IL-1β 可直接誘導原代培養的大鼠星形膠質細胞中 5-HTT 的上調。在 ME/CFS 患者中也檢測到這種促炎細胞因子的濃度非常高,這是由活化的小膠質細胞產生的。
4.1.2 ME/CFS 中QUIN 的產生和NAD+ 代謝
除星形膠質細胞抑制外,QUIN 的過量產生會誘導氧化應激、神經炎症、線粒體功能障礙和細胞死亡。活化的小膠質細胞和浸潤的巨噬細胞是大腦中產生 QUIN 的主要來源。與穀氨酸一樣,QUIN 是 N-甲基-D-天冬氨酸受體 (NMDAR) 的激動劑;因此,它的積累可以在神經元和星形膠質細胞中誘導興奮性毒性。 QUIN 神經毒性的一個有效機制是通過脂質過氧化。更具體地說,QUIN 可以與鐵形成複合物,介導活性氧 (ROS) 和活性氮 (RNS) 的形成,並對脂質、蛋白質和核酸造成氧化損傷。許多研究報導了 ME/CFS 患者的氧化應激水平增加,促進了脂質過氧化和蛋白質羰基的形成。氧化和亞硝化應激誘導內源性表位受損(例如,脂質過氧化的殘留成分),並引發繼發性 IgM 和 IgG 介導的針對新表位的自身免疫反應。 QUIN 還可以增加誘導型一氧化氮合酶 (iNOS) 和一氧化氮 (NO) 產生的活性,這有助於激活大腦中的免疫細胞。與健康人相比,ME/CFS 患者的 iNOS 活性顯著升高。因此,預計這些患者的 NO 產量也會增加。
或者,ME/CFS 患者中過量的 QUIN 產生可能對 NAD+ 代謝產生負面影響。 TRYP 降解代表 NAD+ 產生的從頭途徑,並且在慢性炎症條件下從頭 NAD+ 合成增加。 NAD+ 水平隨著 QUIN 的增加而增加,直至達到喹啉酸磷酸核糖基轉移酶 (QPRT) 發生飽和的水平。 QUIN 的細胞毒性作用已在較高水平上被報導。 NAD+ 在細胞呼吸鍊和其他一些細胞過程(例如鈣穩態、細胞凋亡、衰老、DNA 修復、免疫原性、轉錄調節)中發揮重要作用。幾項研究表明,QUIN 誘導的氧化應激可以過度激活聚(ADP-核糖)聚合酶 (PARP),這是一種在暴露於氧化損傷後修復受損 DNA 的酶。 PARP 過度激活會消耗 NAD+ 和 ATP,並顯著導致線粒體功能障礙、細胞能量損失以及 ROS 和 RNS(例如 NO 和超氧化物)的過度產生,這些在 ME/CFS 中觀察到。
使用反映 ME/CFS 一些臨床特徵的動物模型的研究表明,線粒體複合物表達減少、線粒體形態變化以及最終的線粒體功能障礙與疲勞樣表現、高疼痛敏感性和抑鬱症之間存在密切關聯。最近對 ME/CFS 外周血單個核細胞蛋白質組的所有理論質譜 (SWATH-MS) 分析的序列窗口採集確定了 ME/CFS 中 ATP 和能量產生的明顯下降以及線粒體呼吸鏈中復合物 V 的上調,表明 ROS 產生增加。據報導,ME/CFS 患者存在天然輔酶 Q10 (CoQ10) 和 NADH 的缺陷,即 NAD+ 的還原形式。線粒體氧化磷酸化和 ATP 產生需要最佳水平的輔酶 Q10 和 NADH。
4.1.3 腸道微生物群和ME/CFS
人類微生物群是一個動態群落,由10,000 多種不同的微生物組成,包括細菌、古生菌、病毒、真菌和原生動物。自然地,微生物群是與宿主共同進化的共生或共生菌群,在免疫反應和營養等各種生理過程中發揮著重要作用。更具體地說,人類胃腸道 (GI) 微生物群包含一個複雜的微生物生態系統,可強烈維持胃腸道的穩態。有人提出,胃腸道微生物群的生態失調可能與 ME/CFS 相關。 Giloteaux 等人 報導,與健康對照組相比,ME/CFS 患者的 GI 微生物多樣性較低。該研究還發現 ME/CFS 患者血液樣本中的一些炎症生物標誌物水平較高,包括細菌 LPS、CD14 和 LPS 結合蛋白。例如,IL-1β、IL-6、IL-8 和 TNFα 是一些在 ME/CF 期間增加的促炎細胞因子。另一項研究報告稱,高達 92% 的 ME/CFS 患者患有腸易激綜合徵 (IBS)。
TRYP 可以通過腸道微生物群直接或間接代謝成多種化合物,例如血清素、kYN、吲哚化合物和色胺,它們在腸-腦軸通訊中起重要作用。更具體地說,計算機分析表明,一些 GI 細菌物種(例如擬桿菌門、厚壁菌門、梭桿菌門、放線菌門、變形桿菌門)可以在 GI 系統中分解 TRYP 並產生神經活性代謝物,包括 KYN、KYNA 和 QUIN。與其他胃腸道細菌相比,伯克霍爾德菌屬、雷爾斯頓菌屬、克雷伯氏菌屬和檸檬酸桿菌屬具有將 TRYP 分解代謝為神經活性化合物的更高潛力。微生物吲哚和吲哚衍生化合物(例如,吲哚-3-醛、吲哚-3-乙酸、吲哚-3-丙酸、吲哚-3-乙醛)可以調節 GI 穩態以及 IDO-1 表達。這些吲哚化合物作為信號分子在胃腸道中發揮重要作用,通過與芳烴受體結合,在胃腸道、先天性和適應性免疫系統、各種免疫細胞(如 NK 細胞、T 細胞和巨噬細胞)之間傳遞信息 (AhR) 。吲哚及其衍生物被稱為 AhR 的天然配體,AhR 是一種配體激活的轉錄因子,可介導宿主與微生物群之間的通訊。配體-AhR 複合物被轉運到細胞核中並與 AhR 核轉運蛋白 (ARNT) 蛋白結合,形成異二聚體結構,誘導含有稱為芳烴反應元件 (AhRE) 序列的特定基因。 AhR-ARNT 複合物還可以調節巨噬細胞中 IL-6 的表達。 IL-6 隨後通過 JAK/STAT 信號傳導誘導 IDO-1 的表達,增加 TRYP 代謝物的水平並增強 TRYP 消耗。幾項研究報告了 ME/CFS 患者的 IL-6 水平升高,並在 ME/CFS 症狀的發展中發揮作用。因此,腸道微生物群可能通過食用 TRYP 影響 ME/CFS 患者的 IL-6 水平和炎症。
如前所述,據報導,ME/CFS 患者的腸道微生物多樣性降低。腸道微生物多樣性降低可能會影響外周和中樞神經系統中循環 TRYP 和 KYN 代謝的水平。 Frémont 等人報導了 ME/CFS 患者和健康個體的腸道微生物組成存在顯著差異,擬桿菌門內的 Alistipes 屬數量增加。 Lupo 等人進行的另一項研究報告了 ME/CFS 患者中擬桿菌屬的豐度增加和厚壁菌門(除乳酸因子外)的數量減少。幾種擬桿菌屬(例如 B. thetaiotaomicron、B. ovatus、B. eggerthii、B. fragilis)已被認為在腸道中通過 TRYP 分解代謝產生吲哚及其衍生物。可以假設 ME/CFS 患者 GI 中擬桿菌屬的豐度增加可能會增強 TRYP 代謝和吲哚產生,從而導致 TRYP 耗竭。厚壁菌門的減少可以減少 ME/CFS 患者腸道中短鏈脂肪酸 (SCFA) 的產生。丁酸鹽是一種具有抗炎活性的 SCFA,通過抑制組蛋白去乙酰化酶和降低信號轉導和轉錄激活因子 1 (STAT1) 的表達來降低 IDO-1 轉錄,從而抑制 IFN-γ 依賴性 STAT1 磷酸化並最終降低 STAT1 - 驅動 IDO-1 的轉錄活性。因此,與健康個體相比,由於缺乏產生丁酸鹽的細菌,IDO-1 在 ME/CFS 患者中可能更活躍。
4.1.1 抑鬱和情緒障礙
多項研究提供的證據表明 IDO-1 的過度激活和隨後的 TRYP 消耗可能與抑鬱和其他情緒障礙有關。情緒障礙是 ME/CFS 患者常見的並發症。 IDO-1 在不同的人體組織中廣泛表達,包括腎、腦、肺、樹突狀細胞和巨噬細胞。它由 IFN-γ、TNFα、IL-1β、澱粉樣蛋白 β 和脂多醣誘導。有充分證據表明,情緒障礙與細胞介導的免疫系統激活有關,並伴有炎症增加、IFN-γ、IL-1β 和 TNFα 的產生。這些促炎細胞因子可以強烈激活KP。 KP 的過度激活將 TRYP 從 5-羥色胺生物合成途徑中轉移,從而消耗 5-羥色胺水平,同時刺激 KP 代謝物的過度生產。應該注意的是,KYN 具有抑製作用,而 KYNA 是一種神經保護代謝物。因此,KYN 與 KYNA 的比率是 KAT 活性和神經毒性潛力的重要指標。因此,Maes 等人。 (2011) 報告說,抑鬱症狀,尤其是軀體化,與 KYN:KYNA 和 KYN:TRYP 比率指定的血清 KP 代謝物水平升高直接相關,與血清中血清 TRYP 水平呈負相關.
KYN 向 KYNA 的轉化減少可能是由於神經膠質抑制因子下調 KAT-I 的活性。這種現象會導致 KYN 和 QUIN 水平過高。或者,KYN:KYNA 比率的增加可以通過炎症期間小膠質細胞對星形膠質細胞的影響來證明。在 ME/CFS 患者中廣泛觀察到的慢性炎症會激活小膠質細胞和星形膠質細胞。這些細胞被認為是 TRYP 分解代謝的主要部位 。星形膠質細胞是主要的 KYNA 生產細胞,而小膠質細胞是主要的 QUIN 生產者。小膠質細胞激活誘導大腦中的 KP 並產生促炎介質。激活的小膠質細胞過度產生 QUIN 反過來又通過抑制星形膠質細胞來降低 KYNA 水平。據報導,抑鬱症患者的小膠質細胞數量多,星形膠質細胞滴度低。有人提出小膠質細胞在 ME/CFS 患者的大部分大腦中被激活。因此,Nakatomi 等人 (2014) 報導了與 ME/CFS 患者相比,11C-(R)-PK11195(一種由活化小膠質細胞表達的轉運蛋白的配體)的結合電位值增加。健康的對照。
小膠質細胞激活還可以通過釋放 IL-1β 觸發星形膠質細胞中血清素轉運蛋白 (5-HTT) 的上調,從而降低細胞外血清素水平,從而導致抑鬱症。從小膠質細胞釋放的 IL-1β 與星形膠質細胞 5-HTT 之間的相互作用是眾所周知的,通過使用 IL-1 受體拮抗劑證明了這一點。 IL-1β 可直接誘導原代培養的大鼠星形膠質細胞中 5-HTT 的上調。在 ME/CFS 患者中也檢測到這種促炎細胞因子的濃度非常高,這是由活化的小膠質細胞產生的。
4.1.2 ME/CFS 中QUIN 的產生和NAD+ 代謝
除星形膠質細胞抑制外,QUIN 的過量產生會誘導氧化應激、神經炎症、線粒體功能障礙和細胞死亡。活化的小膠質細胞和浸潤的巨噬細胞是大腦中產生 QUIN 的主要來源。與穀氨酸一樣,QUIN 是 N-甲基-D-天冬氨酸受體 (NMDAR) 的激動劑;因此,它的積累可以在神經元和星形膠質細胞中誘導興奮性毒性。 QUIN 神經毒性的一個有效機制是通過脂質過氧化。更具體地說,QUIN 可以與鐵形成複合物,介導活性氧 (ROS) 和活性氮 (RNS) 的形成,並對脂質、蛋白質和核酸造成氧化損傷。許多研究報導了 ME/CFS 患者的氧化應激水平增加,促進了脂質過氧化和蛋白質羰基的形成。氧化和亞硝化應激誘導內源性表位受損(例如,脂質過氧化的殘留成分),並引發繼發性 IgM 和 IgG 介導的針對新表位的自身免疫反應。 QUIN 還可以增加誘導型一氧化氮合酶 (iNOS) 和一氧化氮 (NO) 產生的活性,這有助於激活大腦中的免疫細胞。與健康人相比,ME/CFS 患者的 iNOS 活性顯著升高。因此,預計這些患者的 NO 產量也會增加。
或者,ME/CFS 患者中過量的 QUIN 產生可能對 NAD+ 代謝產生負面影響。 TRYP 降解代表 NAD+ 產生的從頭途徑,並且在慢性炎症條件下從頭 NAD+ 合成增加。 NAD+ 水平隨著 QUIN 的增加而增加,直至達到喹啉酸磷酸核糖基轉移酶 (QPRT) 發生飽和的水平。 QUIN 的細胞毒性作用已在較高水平上被報導。 NAD+ 在細胞呼吸鍊和其他一些細胞過程(例如鈣穩態、細胞凋亡、衰老、DNA 修復、免疫原性、轉錄調節)中發揮重要作用。幾項研究表明,QUIN 誘導的氧化應激可以過度激活聚(ADP-核糖)聚合酶 (PARP),這是一種在暴露於氧化損傷後修復受損 DNA 的酶。 PARP 過度激活會消耗 NAD+ 和 ATP,並顯著導致線粒體功能障礙、細胞能量損失以及 ROS 和 RNS(例如 NO 和超氧化物)的過度產生,這些在 ME/CFS 中觀察到。
使用反映 ME/CFS 一些臨床特徵的動物模型的研究表明,線粒體複合物表達減少、線粒體形態變化以及最終的線粒體功能障礙與疲勞樣表現、高疼痛敏感性和抑鬱症之間存在密切關聯。最近對 ME/CFS 外周血單個核細胞蛋白質組的所有理論質譜 (SWATH-MS) 分析的序列窗口採集確定了 ME/CFS 中 ATP 和能量產生的明顯下降以及線粒體呼吸鏈中復合物 V 的上調,表明 ROS 產生增加。據報導,ME/CFS 患者存在天然輔酶 Q10 (CoQ10) 和 NADH 的缺陷,即 NAD+ 的還原形式。線粒體氧化磷酸化和 ATP 產生需要最佳水平的輔酶 Q10 和 NADH。
4.1.3 腸道微生物群和ME/CFS
人類微生物群是一個動態群落,由10,000 多種不同的微生物組成,包括細菌、古生菌、病毒、真菌和原生動物。自然地,微生物群是與宿主共同進化的共生或共生菌群,在免疫反應和營養等各種生理過程中發揮著重要作用。更具體地說,人類胃腸道 (GI) 微生物群包含一個複雜的微生物生態系統,可強烈維持胃腸道的穩態。有人提出,胃腸道微生物群的生態失調可能與 ME/CFS 相關。 Giloteaux 等人 報導,與健康對照組相比,ME/CFS 患者的 GI 微生物多樣性較低。該研究還發現 ME/CFS 患者血液樣本中的一些炎症生物標誌物水平較高,包括細菌 LPS、CD14 和 LPS 結合蛋白。例如,IL-1β、IL-6、IL-8 和 TNFα 是一些在 ME/CF 期間增加的促炎細胞因子。另一項研究報告稱,高達 92% 的 ME/CFS 患者患有腸易激綜合徵 (IBS)。
TRYP 可以通過腸道微生物群直接或間接代謝成多種化合物,例如血清素、kYN、吲哚化合物和色胺,它們在腸-腦軸通訊中起重要作用。更具體地說,計算機分析表明,一些 GI 細菌物種(例如擬桿菌門、厚壁菌門、梭桿菌門、放線菌門、變形桿菌門)可以在 GI 系統中分解 TRYP 並產生神經活性代謝物,包括 KYN、KYNA 和 QUIN。與其他胃腸道細菌相比,伯克霍爾德菌屬、雷爾斯頓菌屬、克雷伯氏菌屬和檸檬酸桿菌屬具有將 TRYP 分解代謝為神經活性化合物的更高潛力。微生物吲哚和吲哚衍生化合物(例如,吲哚-3-醛、吲哚-3-乙酸、吲哚-3-丙酸、吲哚-3-乙醛)可以調節 GI 穩態以及 IDO-1 表達。這些吲哚化合物作為信號分子在胃腸道中發揮重要作用,通過與芳烴受體結合,在胃腸道、先天性和適應性免疫系統、各種免疫細胞(如 NK 細胞、T 細胞和巨噬細胞)之間傳遞信息 (AhR) 。吲哚及其衍生物被稱為 AhR 的天然配體,AhR 是一種配體激活的轉錄因子,可介導宿主與微生物群之間的通訊。配體-AhR 複合物被轉運到細胞核中並與 AhR 核轉運蛋白 (ARNT) 蛋白結合,形成異二聚體結構,誘導含有稱為芳烴反應元件 (AhRE) 序列的特定基因。 AhR-ARNT 複合物還可以調節巨噬細胞中 IL-6 的表達。 IL-6 隨後通過 JAK/STAT 信號傳導誘導 IDO-1 的表達,增加 TRYP 代謝物的水平並增強 TRYP 消耗。幾項研究報告了 ME/CFS 患者的 IL-6 水平升高,並在 ME/CFS 症狀的發展中發揮作用。因此,腸道微生物群可能通過食用 TRYP 影響 ME/CFS 患者的 IL-6 水平和炎症。
如前所述,據報導,ME/CFS 患者的腸道微生物多樣性降低。腸道微生物多樣性降低可能會影響外周和中樞神經系統中循環 TRYP 和 KYN 代謝的水平。 Frémont 等人報導了 ME/CFS 患者和健康個體的腸道微生物組成存在顯著差異,擬桿菌門內的 Alistipes 屬數量增加。 Lupo 等人進行的另一項研究報告了 ME/CFS 患者中擬桿菌屬的豐度增加和厚壁菌門(除乳酸因子外)的數量減少。幾種擬桿菌屬(例如 B. thetaiotaomicron、B. ovatus、B. eggerthii、B. fragilis)已被認為在腸道中通過 TRYP 分解代謝產生吲哚及其衍生物。可以假設 ME/CFS 患者 GI 中擬桿菌屬的豐度增加可能會增強 TRYP 代謝和吲哚產生,從而導致 TRYP 耗竭。厚壁菌門的減少可以減少 ME/CFS 患者腸道中短鏈脂肪酸 (SCFA) 的產生。丁酸鹽是一種具有抗炎活性的 SCFA,通過抑制組蛋白去乙酰化酶和降低信號轉導和轉錄激活因子 1 (STAT1) 的表達來降低 IDO-1 轉錄,從而抑制 IFN-γ 依賴性 STAT1 磷酸化並最終降低 STAT1 - 驅動 IDO-1 的轉錄活性。因此,與健康個體相比,由於缺乏產生丁酸鹽的細菌,IDO-1 在 ME/CFS 患者中可能更活躍。
5. NAD+ 作為 ME/CFS 的治療靶點
促炎細胞因子的活性是通過 KP 增加 TRYP 分解代謝的驅動力。因此,旨在抑制促炎細胞因子活性的策略,例如,在 CNS 的外周 IL-6 中合成 IFN-γ 可以抵消 TRYP 的消耗。然而,TRYP 耗竭也代表了使病原體和腫瘤細胞飢餓並促進免疫耐受的重要機制。此外,旨在抑制 KP 的治療策略可以對從頭 NAD+ 合成產生顯著影響。
除了 KP,NAD+ 也可以通過使用前體菸酸 (NA)、煙酰胺 (NAM)、煙酰胺單核苷酸 (NMN) 和煙酰胺核苷 (NR) 的補救途徑產生。然而,應該注意的是,NA 治療會引起一些不希望的負面副作用,包括在低於治療劑量的大多數個體中出現明顯的皮膚潮紅,這限制了其廣泛的臨床應用。 NAM 是肉類中維生素 B3 的主要形式,是 PARP、Sirtuins 和 NAD+ 糖水解酶(例如 CD38)酶促降解 NAD+ 的副產物。 NAM 通過調節單胺神經遞質的合成和降解、有效的抗氧化作用和增加細胞內 NAD+ 水平來幫助從抑鬱症和情緒障礙中恢復[126]。雖然補充 NAM 會提高 NAD+ 而不會引起潮紅,但由於其酶抑制(例如 PARPs、sirtuins、CD38)、甲基消耗和肝毒性潛力,它不太可能成為理想的 NAD+ 補充劑。
NMN 可以從 NR 內源性產生。動物研究表明,NMN 可以改善退化並改善與年齡相關的認知衰退 。然而,NMN 的細胞內攝取尚不清楚。最近,一項研究報告稱,NMN 被去磷酸化為 NR,然後被溶質載體家族 12 成員 8 (Slc12a8) 內化。然而,另一份報告沒有找到足夠的證據支持 Slc12a8 作為“隱匿”的 NMN 轉運蛋白。
NR 是一種前體,可以通過定期食用牛奶自然獲得。 NR 通過 NRK1 和 NRK2 的催化活性轉化為 NAD+。還存在一種 NR 激酶非依賴性途徑,可將 NR 轉化為 NAM,然後將其恢復為 NAD+。 NR 已被證明可以預防認知能力下降和改善大腦減弱大腦退化,並在動物模型中糾正社會缺陷和焦慮症。這表明 NR 可能對 ME/CFS 產生有益影響。據報導,口服 NR 會增加人體全血和組織中的 NAD+ 濃度。 NR 比其他 NAD+ 前體更安全且口服生物利用度更高。與其他菸酸補充劑不同,NR 不會引起潮紅。然而,沒有使用 NAD+ 前體的臨床試驗,特別是 ME/CFS 中的 NMN 和 NR。使用 NMN 和 NR 作為 NAD+ 補充劑來管理和預防 ME/CFS 需要進一步的臨床證據。
限制 NAD+ 和 ATP 水平的線粒體功能障礙是 ME/CFS 患者產生能量的主要因素。補充 CoQ10(200 毫克/天)和 NADH(20 毫克/天)可以增強細胞生物能量,減少疲勞和脂質過氧化物,並改善生化參數(例如,人體中的 CoQ10、ATP、檸檬酸合酶和 NAD+:NADH 氧化還原比)。一項研究顯示,西班牙 CFS 隊列的焦慮和最大心率顯著降低 。另一項研究表明,與安慰劑相比,使用 NADH(10 毫克/天)治療後症狀顯著減輕。在 24 個月內,口服 NADH 補充劑在減輕症狀方面比傳統營養補充劑和心理治療更有效 。口服 NADH 已被證明在人類中是安全的且耐受性良好。然而,CoQ10 的結果是相互矛盾的。一項研究表明,補充 CoQ10(50 毫克/天)和 NADH(5 毫克/天)可顯著降低循環測力計測試期間的最大心率。疲勞感也有所降低,儘管沒有報告疼痛和睡眠有改善 。然而,需要更大規模的對照試驗來證實這些發現。
除了 KP,NAD+ 也可以通過使用前體菸酸 (NA)、煙酰胺 (NAM)、煙酰胺單核苷酸 (NMN) 和煙酰胺核苷 (NR) 的補救途徑產生。然而,應該注意的是,NA 治療會引起一些不希望的負面副作用,包括在低於治療劑量的大多數個體中出現明顯的皮膚潮紅,這限制了其廣泛的臨床應用。 NAM 是肉類中維生素 B3 的主要形式,是 PARP、Sirtuins 和 NAD+ 糖水解酶(例如 CD38)酶促降解 NAD+ 的副產物。 NAM 通過調節單胺神經遞質的合成和降解、有效的抗氧化作用和增加細胞內 NAD+ 水平來幫助從抑鬱症和情緒障礙中恢復[126]。雖然補充 NAM 會提高 NAD+ 而不會引起潮紅,但由於其酶抑制(例如 PARPs、sirtuins、CD38)、甲基消耗和肝毒性潛力,它不太可能成為理想的 NAD+ 補充劑。
NMN 可以從 NR 內源性產生。動物研究表明,NMN 可以改善退化並改善與年齡相關的認知衰退 。然而,NMN 的細胞內攝取尚不清楚。最近,一項研究報告稱,NMN 被去磷酸化為 NR,然後被溶質載體家族 12 成員 8 (Slc12a8) 內化。然而,另一份報告沒有找到足夠的證據支持 Slc12a8 作為“隱匿”的 NMN 轉運蛋白。
NR 是一種前體,可以通過定期食用牛奶自然獲得。 NR 通過 NRK1 和 NRK2 的催化活性轉化為 NAD+。還存在一種 NR 激酶非依賴性途徑,可將 NR 轉化為 NAM,然後將其恢復為 NAD+。 NR 已被證明可以預防認知能力下降和改善大腦減弱大腦退化,並在動物模型中糾正社會缺陷和焦慮症。這表明 NR 可能對 ME/CFS 產生有益影響。據報導,口服 NR 會增加人體全血和組織中的 NAD+ 濃度。 NR 比其他 NAD+ 前體更安全且口服生物利用度更高。與其他菸酸補充劑不同,NR 不會引起潮紅。然而,沒有使用 NAD+ 前體的臨床試驗,特別是 ME/CFS 中的 NMN 和 NR。使用 NMN 和 NR 作為 NAD+ 補充劑來管理和預防 ME/CFS 需要進一步的臨床證據。
限制 NAD+ 和 ATP 水平的線粒體功能障礙是 ME/CFS 患者產生能量的主要因素。補充 CoQ10(200 毫克/天)和 NADH(20 毫克/天)可以增強細胞生物能量,減少疲勞和脂質過氧化物,並改善生化參數(例如,人體中的 CoQ10、ATP、檸檬酸合酶和 NAD+:NADH 氧化還原比)。一項研究顯示,西班牙 CFS 隊列的焦慮和最大心率顯著降低 。另一項研究表明,與安慰劑相比,使用 NADH(10 毫克/天)治療後症狀顯著減輕。在 24 個月內,口服 NADH 補充劑在減輕症狀方面比傳統營養補充劑和心理治療更有效 。口服 NADH 已被證明在人類中是安全的且耐受性良好。然而,CoQ10 的結果是相互矛盾的。一項研究表明,補充 CoQ10(50 毫克/天)和 NADH(5 毫克/天)可顯著降低循環測力計測試期間的最大心率。疲勞感也有所降低,儘管沒有報告疼痛和睡眠有改善 。然而,需要更大規模的對照試驗來證實這些發現。
6. 結論
ME/CFS 是一種知之甚少的疾病,病因不明,沒有既定的診斷標準。在 ME/CFS 期間,NAD+ 水平顯著下降,使患者出現嚴重疲勞。這種下降很大程度上可以解釋為 1) IDO-1 的過度激活將可用的 TRYP 分流到 KP,增加 KP 代謝物,消耗血清素,並導致情緒障礙和其他相關的神經系統症狀; 2) QUIN 在病理生理濃度下可通過興奮性毒性在包括神經元和星形膠質細胞在內的不同細胞中引發氧化應激和細胞凋亡。反過來,較低的星形膠質細胞群會轉化為較低的 KYNA 產量,進一步增強神經系統症狀; 3) 可用的 NAD+ 和 ATP 由於 PARP 的過度激活而耗盡,在 QUIN 誘導的 DNA 氧化損傷之後。這種現象顯著導致細胞能量損失並導致線粒體功能障礙; 4)線粒體功能障礙進一步促進ROS和RNS的產生,導致氧化應激和功能降低; 5)QUIN的積累可以通過引發慢性炎症對上述所有機制進行正反饋控制。這種慢性炎症是由於 QUIN 誘導的大分子損傷、ROS 和 RNS 誘導的內源性表位損傷以及繼發性 IgM 和 IgG 介導的針對新表位的自身免疫反應。通過增加吲哚及其衍生物的產生和改變循環 TRYP 的可用性,腸道微生物群的改變可能進一步促進 ME/CFS。 ME/CFS 患者 GI 中微生物多樣性的減少可能會增加炎症和 IDO-1 活性,從而導致 TRYP 分解代謝和消耗增加。
同樣,提高細胞內 NAD+ 水平可以通過改善神經功能、促進能量產生和降低疲勞來改善生活質量。 NAD+ 前體如 NR 和 NMN 已被建議作為糾正動物模型中焦慮症、疲勞和社交缺陷的潛在治療方法。然而,沒有臨床試驗使用 NAD+ 前體來減輕 ME/CFS 的臨床特徵,需要進一步的臨床評估來使用這些前體來增加 ME/CFS 患者的 NAD+ 水平。使用 NADH 和 CoQ10 的補充劑安全且耐受性良好,可根據全科醫生的建議添加到常規 CFS 治療中。
同樣,提高細胞內 NAD+ 水平可以通過改善神經功能、促進能量產生和降低疲勞來改善生活質量。 NAD+ 前體如 NR 和 NMN 已被建議作為糾正動物模型中焦慮症、疲勞和社交缺陷的潛在治療方法。然而,沒有臨床試驗使用 NAD+ 前體來減輕 ME/CFS 的臨床特徵,需要進一步的臨床評估來使用這些前體來增加 ME/CFS 患者的 NAD+ 水平。使用 NADH 和 CoQ10 的補充劑安全且耐受性良好,可根據全科醫生的建議添加到常規 CFS 治療中。