中國研究表明骨骼形成需要 NMN (2022/02)
2022年2月四川大學的研究(doi: 10.1186/s13287-022-02748-9. PMID: 35193674; PMCID: PMC8864833.)表明,NAD+是骨髓幹細胞修復骨折所不可或缺的。
重點
1.在人類中,NMN 是骨幹細胞成熟為稱為成骨細胞的骨生成細胞所必需的。
2.增強 NMN 合成可促進骨幹細胞成熟,產生更多成骨細胞,並促進骨形成。
3.阻斷 NMN 合成通過抑制骨幹細胞發育成骨生成細胞來損害小鼠的骨折修復。
重點
1.在人類中,NMN 是骨幹細胞成熟為稱為成骨細胞的骨生成細胞所必需的。
2.增強 NMN 合成可促進骨幹細胞成熟,產生更多成骨細胞,並促進骨形成。
3.阻斷 NMN 合成通過抑制骨幹細胞發育成骨生成細胞來損害小鼠的骨折修復。
當我們骨折時,我們骨髓中的幹細胞會設計一個多階段的過程來修復和治愈骨折。 骨髓中的這些幹細胞稱為骨間充質幹細胞 (BMSCs),對骨再生至關重要。 骨折癒合延遲或失敗,發生在 5-10% 的病例中,通常可以追溯到 BMSC 活性不足或功能失調。
中國四川大學的研究人員報告說,提高 NAD+ 水平對於 BMSC 產生稱為成骨細胞的成骨細胞並形成骨骼是必不可少的。 在哺乳動物中,NAD+ 主要由 NMN 通過一種稱為 NAMPT 的酶合成。 Li 及其同事表明,阻斷 NAMPT 可阻止人類 BMSCs 成熟為成骨細胞並減少骨形成。 另一方面,通過增強 NAMPT 活性來提高 NAD+ 水平會增加 BMSC 成熟為成骨細胞並刺激骨形成。 這種範例適用於培養皿中的細胞和動物,因為在活小鼠中阻斷 NAMPT 會抑制骨折修復。 該研究發表在《幹細胞研究與治療》上,表明 NAD+ 可能為骨修復和再生提供潛在的治療靶點。
更好地重建骨骼
BMSCs 目前被用作組織再生和幹細胞治療的種子細胞。這些可自我更新的細胞有可能分化成多種類型的細胞,包括成骨細胞和產脂肪細胞(脂肪細胞)。 BMSCs 以一種相互排斥的方式轉化為這些細胞——也就是說,它們通常成熟為這兩個譜系中的一個。了解如何調整尺度以控制 BMSC 向成骨細胞成熟對骨修復具有重大影響。
多種因素有助於 BMSCs 向骨骼或脂肪形成的譜系承諾,包括細胞外環境和細胞代謝。細胞產生能量的主要途徑,氧化磷酸化,是線粒體最關鍵的代謝活動之一。細胞還可以通過糖酵解在細胞質中產生能量——這種產生能量的方式比氧化磷酸化效率低;通過線粒體氧化磷酸化的糖代謝可以產生比糖酵解多十五倍的能量。但對於氧化磷酸化和糖酵解在調節 BMSCs 細胞命運決定和成熟中的作用知之甚少。
人體骨骼形成依賴於 NMN 產生的 NAD+
Li 及其同事旨在梳理 BMSCs 譜系確定過程中代謝和 NAD+ 的作用。 四川大學的研究人員表明,培養的人骨髓間充質幹細胞正在成熟為骨生成細胞,其代謝從糖酵解轉變為氧化磷酸化。 與增強的氧化磷酸化相一致,線粒體在骨形成(成骨)期間變得細長並且數量顯著增加。 相反,致力於成熟為產脂肪細胞的 BMSCs 表現出整體代謝增加,氧化磷酸化和糖酵解活性增加。
中國四川大學的研究人員報告說,提高 NAD+ 水平對於 BMSC 產生稱為成骨細胞的成骨細胞並形成骨骼是必不可少的。 在哺乳動物中,NAD+ 主要由 NMN 通過一種稱為 NAMPT 的酶合成。 Li 及其同事表明,阻斷 NAMPT 可阻止人類 BMSCs 成熟為成骨細胞並減少骨形成。 另一方面,通過增強 NAMPT 活性來提高 NAD+ 水平會增加 BMSC 成熟為成骨細胞並刺激骨形成。 這種範例適用於培養皿中的細胞和動物,因為在活小鼠中阻斷 NAMPT 會抑制骨折修復。 該研究發表在《幹細胞研究與治療》上,表明 NAD+ 可能為骨修復和再生提供潛在的治療靶點。
更好地重建骨骼
BMSCs 目前被用作組織再生和幹細胞治療的種子細胞。這些可自我更新的細胞有可能分化成多種類型的細胞,包括成骨細胞和產脂肪細胞(脂肪細胞)。 BMSCs 以一種相互排斥的方式轉化為這些細胞——也就是說,它們通常成熟為這兩個譜系中的一個。了解如何調整尺度以控制 BMSC 向成骨細胞成熟對骨修復具有重大影響。
多種因素有助於 BMSCs 向骨骼或脂肪形成的譜系承諾,包括細胞外環境和細胞代謝。細胞產生能量的主要途徑,氧化磷酸化,是線粒體最關鍵的代謝活動之一。細胞還可以通過糖酵解在細胞質中產生能量——這種產生能量的方式比氧化磷酸化效率低;通過線粒體氧化磷酸化的糖代謝可以產生比糖酵解多十五倍的能量。但對於氧化磷酸化和糖酵解在調節 BMSCs 細胞命運決定和成熟中的作用知之甚少。
人體骨骼形成依賴於 NMN 產生的 NAD+
Li 及其同事旨在梳理 BMSCs 譜系確定過程中代謝和 NAD+ 的作用。 四川大學的研究人員表明,培養的人骨髓間充質幹細胞正在成熟為骨生成細胞,其代謝從糖酵解轉變為氧化磷酸化。 與增強的氧化磷酸化相一致,線粒體在骨形成(成骨)期間變得細長並且數量顯著增加。 相反,致力於成熟為產脂肪細胞的 BMSCs 表現出整體代謝增加,氧化磷酸化和糖酵解活性增加。

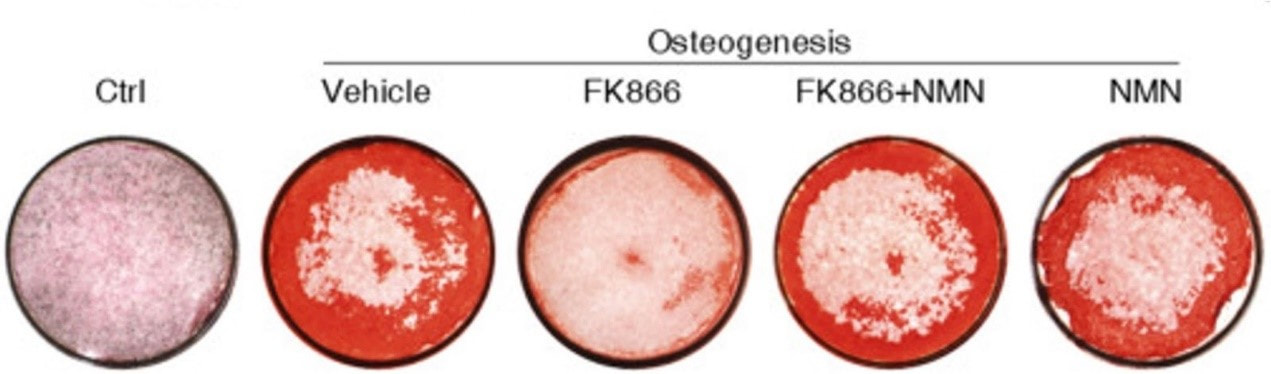
(Li et al., 2022 | Stem Cell Research & Therapy) 增強 NAMPT 活性可增加成體幹細胞生成的骨骼。 一方面,通過 P7C3 增強 NAMPT 促進人 BMSCs 成為成骨細胞並形成骨骼(成骨)。 另一方面,通過 FK866 抑制 NAMPT 可抑制人骨髓間充質乾細胞的成骨並消除由茜素紅染色的礦化結節的形成。 ALP(鹼性磷酸酶)和 AR(茜素紅)染色分別為藍色和紅色的骨形成。
他們還發現 NAD+ 是 BMSCs 選擇成骨命運的關鍵。當 Li 及其同事通過使用 NAMPT 抑製劑 (FK866) 抑制 NAD+ 合成來降低 NAD+ 水平時,他們觀察到成骨細胞成熟和骨生成受損。當 NAMPT 激活劑 (P7C3) 提高 NAD+ 水平時,這些影響被逆轉。此外,這項研究表明,在 BMSC 成熟為骨生成細胞期間,NAD+ 是維持線粒體功能和氧化磷酸化活性所必需的。通過阻斷 NAMPT 來抑制 NAD+ 會損害線粒體融合,導致線粒體功能障礙和氧化磷酸化活性降低,從而停止骨生成。
由於 NMN 是 NAMPT 的直接產物,Li 及其同事研究了 NMN 是否可以減輕 NAMPT 對成骨細胞生成的抑制並挽救線粒體功能。 NMN 治療部分恢復了通過抑制 NAMPT 抑制的成骨細胞生成和骨形成。值得注意的是,NMN 顯著阻止了由 NAMPT 抑制引起的線粒體健康和功能下降。這些數據表明,通過抑制 NAMPT 來阻斷 NAD+ 合成會抑制 BMSC 成骨,這可以通過補充 NMN 來部分恢復
小鼠的骨修復依賴於 NMN 產生的 NAD+
為了評估 NAD+ 在小鼠成骨中的作用,Li 及其同事進行了骨折模型實驗並註射了 NAMPT 抑製劑 FK866。 與細胞培養數據一致,四川大學的研究人員表明,當 NAMPT 受到抑制時,骨折癒合受到抑制,軟骨和骨骼的形成受損。 此外,FK866 治療降低了癒傷組織的礦物質密度——骨和軟骨材料在修復過程中形成跨越骨折的連接橋。
由於 NMN 是 NAMPT 的直接產物,Li 及其同事研究了 NMN 是否可以減輕 NAMPT 對成骨細胞生成的抑制並挽救線粒體功能。 NMN 治療部分恢復了通過抑制 NAMPT 抑制的成骨細胞生成和骨形成。值得注意的是,NMN 顯著阻止了由 NAMPT 抑制引起的線粒體健康和功能下降。這些數據表明,通過抑制 NAMPT 來阻斷 NAD+ 合成會抑制 BMSC 成骨,這可以通過補充 NMN 來部分恢復
小鼠的骨修復依賴於 NMN 產生的 NAD+
為了評估 NAD+ 在小鼠成骨中的作用,Li 及其同事進行了骨折模型實驗並註射了 NAMPT 抑製劑 FK866。 與細胞培養數據一致,四川大學的研究人員表明,當 NAMPT 受到抑制時,骨折癒合受到抑制,軟骨和骨骼的形成受損。 此外,FK866 治療降低了癒傷組織的礦物質密度——骨和軟骨材料在修復過程中形成跨越骨折的連接橋。
(Li et al., 2022 | Stem Cell Research & Therapy) NMN 是成體幹細胞生成骨骼所必需的。 NAMPT 抑製劑 FK866 阻斷了來自人 BMSCs 的成骨細胞(成骨細胞(染成紅色)的形成)。 NMN是NAMPT活性的輸出,克服了FK866的抑製作用,恢復了BMSCs的成骨能力。
NAD+ 促進可以改善骨骼修復嗎?
檢查補充 NAD+ 或其中間體是否有益於骨折修復將是一件有趣的事情。 Li 及其同事的工作與最近關於 NMN 和骨骼健康與生產的其他工作是一致的。 例如,幾週前發表的一項研究表明,NMN 可以通過防止衰老來重振骨髓間充質乾細胞的“乾性”——這是一種細胞不再生長或複制的與年齡相關的疾病。 2020 年,另一項研究揭示了 NMN 治療作為治療衰老小鼠骨質疏鬆症的潛在聯繫。 這種數據的融合可能會促使人們冒險研究 NMN 在人類骨骼形成和再生方面的治療潛力。
檢查補充 NAD+ 或其中間體是否有益於骨折修復將是一件有趣的事情。 Li 及其同事的工作與最近關於 NMN 和骨骼健康與生產的其他工作是一致的。 例如,幾週前發表的一項研究表明,NMN 可以通過防止衰老來重振骨髓間充質乾細胞的“乾性”——這是一種細胞不再生長或複制的與年齡相關的疾病。 2020 年,另一項研究揭示了 NMN 治療作為治療衰老小鼠骨質疏鬆症的潛在聯繫。 這種數據的融合可能會促使人們冒險研究 NMN 在人類骨骼形成和再生方面的治療潛力。